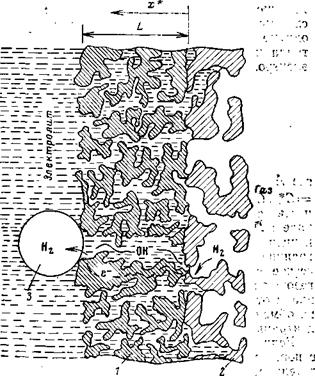
НАРУШЕНИЕ МАССОПЕРЕНОСА И НЕСТАБИЛЬНОСТЬ СТРУКТУРЫ ВОДОРОДНЫХ И КИСЛОРОДНЫХ ЭЛЕКТРОДОВ
НАРУШЕНИЕ МАССОПЕРЕНОСА И НЕСТАБИЛЬНОСТЬ СТРУКТУРЫ ВОДОРОДНЫХ И КИСЛОРОДНЫХ ЭЛЕКТРОДОВ
В подпараграфе 3.1.1 подробно рассмотрены принципы построения электродов различного типа, а также конструкционные особенности наиболее распространенных газодиффузионных электродов. Эти электроды представляют собою многослойную композицию, которая осуществляет следующие функции: разделение газового и жидкостного компонентов, создание трехфазной границы, на которой протекает реакция, транспорт газа в зо-
157
ну реакции, отвод ионизированных продуктов анодной и катодной реакций в электролит, вывод электронов во внешнюю электрическую цепь и отвод окончательного продукта реакции. Эффективность разделения газового и жидкостного компонентов влияет на функциональную работоспособность электрода, а стабильность структуры активного и запорного слоев определяет его ресурсные характеристики.
Работа ТЭ с жидким свободным электролитом иногда сопровождается появлением газовых пузырьков в привлек! родном пространстве. Увеличение объема газовой фазы в электролите всегда нежелательно, а в некоторых ■случаях полностью определяет возможную продолжительность работы топливного элемента. Очевидно, что в случае гидрофильного запорного слоя это явление может быть связано с нарушением нормальной работы запорного слоя электрода, когда часть его пор свободна от жидкости, образуя сквозной канал для пробульки — вающего газа. Общие условия появления сквозных газовых пор обсуждаются, в частности, в [3.34]. В дополнение к пробулькиванию описаны также механизмы диффузионного и миграционного натекания. Последнее связано с явлением капиллярного гистерезиса. Периодическое изменение давления (или условий смачивания) приводит к появлению защемленных жидкостью пузырей таза, которые, совершая хаотические блуждания, могут проникать в электролитную камеру. Практически удастся полностью избавиться от пробулькивания и миграционного натекания выбором технологических и эксплуатационных параметров. Диффузионное натекание, происходящее за счет переноса газа в растворенном состоянии через поры, заполненные жидкостью, было исследовано в [3.35].
Концентрация растворенного газа у мениска жидкостной поры пропорциональна давлению газа в газовой фазе; в активном слое противоположного электрода концентрация газа близка к нулю. Концентрация растворенного газа вблизи газового пузыря пропорциональна давлению в нем. Диффузионное натекание связано лишь с ростом пузырей в электролитной камере после превышения ими определенного критического размера. При •отсутствии газовых пузырей стационарного диффузионного натекания происходить не будет, хотя электролит пересыщен растворенным газом.
Из условия механического равновесия пузыря с электролитом можно записать
(Гп)крг^2<т/ (рк Рэ) > (3.46)
где га — радиус пузыря; рк — давление в газовой камере; рэ —давление электролита.
Пузырек газа радиусом больше критического будет расти за счет диффузионного потока в него. Предполагая, что концентрация растворенного газа линейно уменьшается до нуля у противоположного электрода, можно определить область вблизи активного слоя, в которой возможен рост пузырей:
![]()
![]()
![]() (3.47)
(3.47)
где Рп — равновесное давление водяных паров; Л — расстояние между активными слоями электродов.
Минимальное давление водяного пара, при котором область возможного существования пузырей не ограничивается запорным слоем t^d, находится из условия
![]()
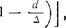
 |
(3.48)
где р°=Рк—Рп — парциальное давление газа в газовой камере; D и В — истинный и эффективный коэффициенты диффузии газа в электролите; k — константа растворимости Генри.
В последнем выражении предполагается, что весь электролит на границе с активным слоем полностью насыщен газом. Однако такое предположение может быть сделано лишь в отсутствие тока. Если через элемент идет ток, то участки тыльной поверхности активного — слоя между газовыми порами служат стоками натекающего из газовых пор газа. Предполагая диффузионный режим работы электрода, можно считать, что растворенный газ исчерпывается на расстоянии б (рис. 3.36) от стенки газовой поры.
Тогда средняя по рассматриваемой поверхности концентрация газа (в линейном приближении)
ПРИ s<6;
![]() с = C0 при 5 3= b,
с = C0 при 5 3= b,
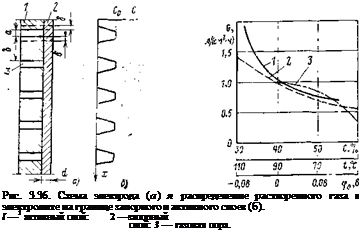 |
где a — средняя ширина газовых пор; b — расстояние между газовыми порами; Са — концентрация растворен-
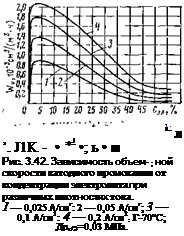
Рис. 3.37. Зависимость относительной плотности потока натекания G от концентрации электролита С (/), температуры t (2) и поляризации электрода фо (3).
ного газа у границы раздела фаз; диффузионная длина
п — заряд иона; F — число Фарадея; /о — плотность тока обмена; s — удельная поверхность; R — газовая постоянная; Г —температура; фо — поляризация электрода.
Максимальная плотность потока диффузионного натекания при наличии тока с учетом (3.50)
![]()
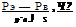
![]()
фА+б&у,
Dlki £*2&2
где 6i и Ь-2 — диффузионные длины каждого электрода.
На рис. 3.37 приведены относительные плотности потока диффузионного натекания G, рассчитанные по вышеприведенным формулам. За единицу принято натекание при 90°С, давлении газа 0,13 МПа и концентрации электролита 40%.
Экспериментальные исследования на водородно-кислородных ТЭ, выполненные авторами, показали, что по составу натекающий газ практически полностью состоит из водорода, а также скорости его переноса значительно выше тех, которые получаются при оценках диффузионных потоков. К тому же было замечено, что при неизменных внешних физических параметрах и одинаковых структурных характеристиках электродов потоки натекания значительно различаются, что не может най-
|
Рис. 3.38. Схема переноса водорода через запорный слой электрода. 1 — запорный слой; г—активный слой; 3—-пузырек водорода. |
![]()
ти себе объяснение лишь в рамках диффузионной теории переноса. Было высказано предположение [3.36], что для некоторых газовых реагентов наряду с указанным диффузионным может присутствовать и электрохимический механизм переноса. Остановимся на электрохимической стороне явления.
Различные концентрации растворенного в электролите газа на противоположных сторонах запорного слоя электрода навязывают различные электрические потенциалы соответствующим участкам его материала. Если этот материал обладает электронной электропроводностью, то в нем работает газовый концентрационный ТЭ, замкнутый накоротко металлом запорного слоя (рис. 3.38).
 Процессы переноса в участке газозапорного слоя,
Процессы переноса в участке газозапорного слоя,
= С*Н/С°Н; /=/*//о; ф=2FV/RT; s — удельная поверхность запорного слоя; L — его толщина; F— число Фарадея; В — эффективный коэффициент диффузии; С°н— концентрация молекулярного водорода в электролите на границе с газом газовой камеры; р — удельное электрическое сопротивление электролита; R — универсальная газовая постоянная; Т — температура; V— сдвиг потен-*, циала от равновесного при С*ц=С°н; /о— плотность тока обмена при С=1; /* — фарадеевский ток; С*„ — кон-, центрация водорода в электролите; х* — координата.
Если омическое падение потенциала в электролите в порах против пузырька значительно меньше разности потенциалов по обеим сторонам запорного слоя
пт
(/*)срРЕ<-т[1пС,, ■
где (/*)ср — средняя по толщине запорного слоя njlof — иость тока, a Ci=C при Х=1, то омическое падение потенциала не может существенно сказаться на процессах переноса н можно положить потенциал электролита постоянным. Тогда система (3.53) сведется йодному уравнению
^ = Л[)/Сехр(<р) —ехр (—?)]. (3.54)
Если ограничиться областью малого превышения давления в газовой камере над давлением электролита (С’-=1), то уравнение (3.54) может быть заменено нижеследующим, допускающим аналитическое решение,
![]() ехр (у) — ехр (— 9)|. (3.55)
ехр (у) — ехр (— 9)|. (3.55)
Решение уравнения (3.55) с граничными условиями С=1 при Х=0 и С=Сі при х— имеет вид
C=2{ir? K1-a)shni-^) + (C,-«)slipX] + «-l},
(3.56)
где а — ехр (— 2<р); (З2 — /Т’2ехр(<р).
Уравнение (3.55) позволяет рассчитать поля концентраций и оценить поток к пузырьку. Максимальный электрохимический перенос будет иметь место при
Это условие позволяет определить у=90 при (/*) =
1 2
— О и а0^=(1 —|— С)/2; <р0 = -у InсГ+Т • Максимальный поток
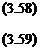
![]() fiC^dC L dX>
fiC^dC L dX>
°.=5тЧ*їг1(сіір.+’)’
или
q __ go (eh go Ч— 1)
0 лі’* 2sh go
—■ С,) — поток молекулярной диффуз ИИ.
и
■ Увеличение переноса за счет электрохшййческих процессов определяется коэффициентом
![]() где
где
, Р
На рис. 3.39 представлены поля концентрации растворенного газа, определенные по (3.56), а также рассчитанные на ЭВМ по системе (3.53).
На рис. 3.40 показан вклад электрохимических процессов в переносе газа. Уравнение (3.61) показывает,
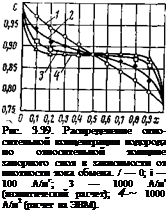 что перенос через «малоактивные» запорные слои (/о= 10“’ А/м2; А=1) хорошо описывается молекулярным механизмом (G=tel).
что перенос через «малоактивные» запорные слои (/о= 10“’ А/м2; А=1) хорошо описывается молекулярным механизмом (G=tel).
Для «активных» запорных слоев (/0=10 А/м2; А = 100) перенос определяется электрохимическими процессами (G=10). Различие в результатах аналитического и численного решений, представленных на рис. 3.39 и 3.40, отражает в основном влияние электрического сопротивления электролита. Как видно, определяющее влияние на электрохимический перенос водорода через электрод оказывает активность его запорного слоя. Хотя на практике при изготовлении катализатор специально не вносится в запорный слой, однако в про-1 цессе длительной эксплуатации или нарушения режимов хранения ТЭ в заправленном состоянии возможно попадание дисперсного катализатора на тыльную сторону запорного слоя водородного электрода. Аналогичные выводы были сделаны в [3.37], где исследован эффект «электрохимического перетекания» водорода на близких по конструкции газодиффузионных электродах.
Процесс аномального газопереноса наблюдается также в электродах с гидрофобным гидрозапорным слоем при наличии положительного градиента давления со сто — 64
роны жидкости. Исследование самопроизвольного про — булькивания газа через электроды такого типа показало, что явление не зависит от протекающих электрохимических процессов и связано с физическими свойствами пористых сред, а именно структурными характеристиками гидрофобной части электрода [3.38].
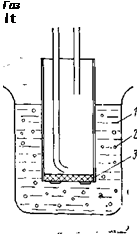 Если лиофобная микропористая мембрана одной стороной обращена к летучей жидкости, а другой к газу, то газ может протекать через мембрану и самопроизвольно пробульки — вать через жидкость против значительного давления при условии, что поры достаточно малы и выполняются некоторые необходимые условия (рис. 3.41). Если к мембране подходит псг’К сухого газа, подогретого до температуры жидкости, про — булькивание устойчиво. Если газ подогрет и насыщен парами при температуре жидкости, пробулькивание прекращается. Скорость пробулькивания тем меньше, чем меньше летучесть жидкости (летучесть пропорциональна давлению насыщенных паров) . С ростом температуры жидкости скорость пробулькивания возрастает.
Если лиофобная микропористая мембрана одной стороной обращена к летучей жидкости, а другой к газу, то газ может протекать через мембрану и самопроизвольно пробульки — вать через жидкость против значительного давления при условии, что поры достаточно малы и выполняются некоторые необходимые условия (рис. 3.41). Если к мембране подходит псг’К сухого газа, подогретого до температуры жидкости, про — булькивание устойчиво. Если газ подогрет и насыщен парами при температуре жидкости, пробулькивание прекращается. Скорость пробулькивания тем меньше, чем меньше летучесть жидкости (летучесть пропорциональна давлению насыщенных паров) . С ростом температуры жидкости скорость пробулькивания возрастает.
Явление пробулькивания газа связывалось с существованием стефановского потока пара от жидкости к газу через капилляры. Из соображений размерности была оценена скорость массопереноса и соответствующий ей (по формуле Пуазейля) перепад дав-
Рис. 3.41. Пробулькивание газа
в жидкость.
/ — жидкость; 2 — пузырьки газа; 3 — по-
ристая лиофобная мембрана.
![]()
Ленин в поре, а из рассмотрения устойчивости капиллярного мениска рассчитано критическое капиллярное давление [3.39]. Движущей силой эффекта пробулькивания также назывался градиент парциального давления газа, вызываемый наличием градиента парциального давления паров жидкости от границы раздела газа и жидкости к открытым концам пор мембраны.
Была решена задача диффузии бинарной газовой смеси в пористом теле с учетом изменения общего давления. Предложенное описание имеет статистическое обоснование и удовлетворительную физическую интерпретацию полученных предельных выражений. Последовательная количественная теория явления на примере пористой фторопластовой мембраны, разделяющей воздух и воду, изложена в [3.40].
Поровое пространство мембраны заполнено бинарной газовой смесью, давление которой равно pi+pz, где pi— парциальное давление паров воды, а р% — парциальное давление воздуха. Парциальное давление насыщенных паров воды p°i на стороне мембраны, граничащей с водой, определяется ее температурой, а на «газовой» стороне мембраны в условиях достаточного конвективного обмена воздуха может быть принято равным нулю. В стационарном случае источников и стоков нет, поэтому поток воздуха повсюду равен нулю и в соответствии с оценками течение может считаться пуазейлевским. Так как р°і задано, то для того, чтобы оценить перепад суммарного давления смеси на границе газ — жидкость, необходимо рассчитать соответствующее парциальное давление воздуха р°%.
Уравнение для р° имеет вид
. -2аIn/>% = (/, +Л)*- 1, (3.62)
где
__ TpD(p1 + рг) Df]
а — — T*Dp2Kl
— безразмерный параметр задачи; pi и рг — давления на «газовой» стороне мембраны; D — коэффициент взаимной диффузии; Т — температура; ц —динамическая вязкость паров воды; К— газовая проницаемость пористой среды; I — извилистость пор; TD и pD — температура и давление, при которых взято значение D.
Так как коэффициент диффузии обратно пропорционален суммарному давлению, то D(pi+p2)—величина постоянная и, следовательно, о зависит только от Т.
При а-Ч), что соответствует бесконечной газовой проницаемости К,
(р°1+р°2)-Ч, (3.63)
т. е. давление газовой смеси на границе с жидкостью равно давлению на газовой стороне в силу того, что конвективные потоки быстро выравнивают градиент суммарного давления.
При а-^оо, что соответствует нулевой проницаемости (и увеличению влияния пористого тела),
p°r+1 (3.64)
и
(Р°1+Р02)^(1+Р°і), (3.65)
т. е. давление на границе с жидкостью превышает давление на газовой стороне на парциальное давление насыщенных паров воды.
В реальном случае при конечных значениях
K(p0i+p02)<(l+P°i). (3.66)
т. е. имеется некоторый перепад давления, который и вызывает пробулькивание.
Не меньший физический интерес и практическую трудность устранения представляет явление катодного промокания, которое первоначально было обнаружено у гидрофобных воздушных электродов. Оно заключается в постепенном заполнении газового порового пространства электрода щелочным электролитом и сопровождается падением электрохимической активности. Образование капель на активном слое катодов наблюдалось А. Клаусом и др. в батарее ТЭ при подаче в нее топлива и окислителя. Капли жидкости появлялись на катоде за время, варьировавшееся от нескольких минут до часа. При этом анод оставался совершенно сухим. Оба электрода ТЭ были сделаны одинаково, и если менялись местами топливо и окислитель, то электрод, бывший ранее катодом, становился сухим со стороны газа, а новый катод начинал запотевать. Причиной этого явления был назван электроосмос, однако это вызывает существенные возражения. Электроосмос в концентрированных электролитах, таких как раствор 6 М КОН, невозможен, так как потенциал практически равен нулю.
Было замечено, что скорость образования капель электролита пропорциональна току нагрузки. Это явление наблюдалось также и тогда, когда один из электродов доходил до потенциала выделения водорода. Концентрация электролита в каплях приблизительно в 2 раза больше, чем в основном объеме. В качестве объяснения этого явления были приведены суждения о соотношении диффузии воды и гидратированных катионов К(Н20)+4 в жидкостных порах электрода. Отношение коэффициентов диффузии воды и щелочи пропорционально отношению их молекулярных масс и равно 3,1. Пренебрегая изменением плотности в ходе реакции и предполагая, что массоперенос КОН протекает в стационарных условиях, получаем:
выход Н20=(3,1/+—0,5)I/F, (3.67)
где t+—число переноса катиона, а 0,51/F — количество воды, потребляемой в катодной реакции.
Если ^+>0,16, то появление воды внутри поры будет вызывать увеличение КОН внутри поры вследствие уменьшенной диффузии КОН. Избыток КОН будет приводить к затоплению пор. Принимая во внимание изменение плотности в диапазоне между 5 н и 10 н КОН, получаем
выход Н20=(1,Н+—0,5)I/F. (3.68)
Промоканию благоприятствует наличие в электроде очень малых пор, которые требуют значительного давления для создания обратного гидравлического потока.
Может быть дано и другое объяснение явления. Движущей силой эффекта промокания является градиент парциального давления водяного пара в порах, приводящий к изотермической дистилляции. Давление пара над раствором уменьшается с увеличением концентрации растворенного вещества. В тех порах электрода, где концентрация электролита возрастает во время прохождения тока, вода испаряется из менее концентрированного раствора на электролитной стороне и конденсируется в более концентрированном растворе на газовой стороне. Таким образом, в порах возникает градиент парциального давления водяного пара с результирующей
диффузией по направлению к газовой стороне. За счет этого объем электролита в порах на газовой стороне увеличивается, вызывая давление, которое выталкивает часть электролита из этих пор на газовую сторону в виде капель.
 |
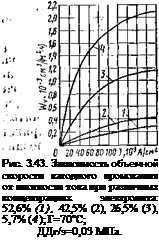 |
Приведенное объяснение механизма промокания хорошо согласуется с наблюдаемыми зависимостями скорости промокания от тока нагрузки (рис. 3.42) и концентрации электролита (рис. 3.43).
Однако выполненные нами дополнительные экспери-,: ментальные исследования поведения промокающих электродов с гидрофильным запорным и іидрофобизирован — ным активным слоями, работающих со значительным перепадом давления газ — электролит (до 0,07 МПа), с помощью методов микрокиносъемки (рис. 3.44) заставляют усомниться в корректности предложенного механизма процесса. Оказалось, что электроды промокают тогда, когда не протекает электрохимическая реакция, но с поверхности электрода на газовой стороне происходит испарение воды. И это промокание тем интенсив — нее, чем выше скорость испарения. И наоборот, под то — ’ ком нагрузки подача на реакцию увлажненного газа способна полностью прекратить процесс промокания.
Эти исследования, а также исследования динамического поведения пленок электролита на полупогружен-
Рис. 3.44. Капли электролита на га-
зовой стороне электрода («промока-
ние»).
 ных электродах позволили предположить следующий механизм процесса промокания.
ных электродах позволили предположить следующий механизм процесса промокания.
Пленка электролита в зоне трехфазной границы получает подвижность в направлении к газу за счет сил поверхностного натяжения, градиент которых появляется за счет возникновения градиента концентрации. Поверхностное натяжение для раствора КОН увеличивается с увеличением концентрации dajdC=2,4 • 10 3 Н*м_1Х Хмоль-1 при 18°С в диапазоне З М<С<;12,5 М. Известно, что достаточно очень небольшого градиента поверхностного натяжения, чтобы вызвать заметное движение тонких пленок. Учитывая то, что внутренняя поверхность порового пространства активного слоя электрода представляет собой мозаичную структуру из гидрофильных гранул катализатора и гидрофобных участков пластмассового связующего, можно предположить, что в некоторых местах складываются условия для дробления пленок на отдельные мелкие (первичные) капли электролита. Поскольку этот процесс идет непрерывно, то первичные капли агрегатируются в более крупные, положение которых внутри активного слоя определяется как результат взаимодействия отдельных капиллярных сил ограничивающих их менисков электролита. Часть этого электролита должна возвращаться в основной его объем (в нормально смоченную зону электрода), а другая может выходить на газовую сторону. Очевидно, что интенсивность этого процесса определяется скоростью генерации первичных капель и соотношением гидрофильных и гидрофобных поверхностей в структуре активного слоя электрода. Количественное описание предложенного механизма процесса промокания представляет определенные трудности, однако развитые модельные представления не только качественно хорошо согласуются со всей суммой экспериментально наблюдаемых фактов, но и позволили разработать электроды, в которых этот процесс локализован в активном слое и не оказывается на функциональной работоспособности.
ГЛАВА ЧЕТВЕРТАЯ