МЕТОДЫ ПРЕДОТВРАЖЕНИЯ ОБРАЗОВАНИЯ ОТЛОЖЕНИЙ
МЕТОДЫ ПРЕДОТВРАЖЕНИЯ ОБРАЗОВАНИЯ ОТЛОЖЕНИЙ
Необходимость обработки воды для предотвращения образования карбонатных и иных отложений в проектах систем оборотного водоснабжения надлежит устанавливать на основе опыта эксплуатации аналогичных систем на воде данного источника водоснабжения или предварительных исследований на модели системы оборотного водоснабжения с учетом конкретных условий.
При отсутствии опыта эксплуатации и данных экспериментальных исследований обработку охлаждающей воды следует предусматривать при восполнении систем водой: из подземных источников при ее карбонатной жесткости (щелочности) свыше 1,5 мг-экв/дм3; из поверхностных источников — рек и водохранилищ средней полосы или очищенными сточными водами — свыше 2,5 мг-экв/дм3; из рек и водохранилищ северных районов, а также горно-ледниковым питанием — свыше 3,5 мг-экв/дм3. При карбонатной жесткости добавочной воды менее указанных значений можно предусматривать только освежение оборотной воды (продувку системы) путем непрерывного сброса части ее и замены водой из источника с использованием продувочных вод в циклах, не предъявляющих особых требований к качеству водьі.
В состав отложений минеральных солей входят: CaC03, MgC03, MgSiO, CaS04, BaS04, Mg(OH)2, Fe(OH)2, Fe(OH)3, CaF2, FeS, а также гидроксиды и сульфиды тяжелых металлов.
|
Концентрация комтшексої іа} мг/ом5 |
Удельная поверхностная энергия (х 10’), Дж/м2 |
Радиус Критического іародЬі1и им |
|
0 |
4,0 |
0,25-0,27 ——————— |
|
1,0 |
8,9 |
0,25-0,54 |
|
2,0 |
11,2 |
0,6-0,66 |
Борьбу с отложениями карбоната кальция в теплообменных аппаратах и тру. бопроводах систем оборотного водоснабжения можно вести следующими традиционными способами:
• непрерывным добавлением в систему оборотного водоснабжения воды с меньшей карбонатной жесткостью при сбросе части отработавшей (оборотной) воды из системы (продувкой);
• подкислением;
• добавлением в оборотную поду веществ, тормозящих процесс кристаллизации карбоната кальция (фосфатирование);
• совместной обработкой воды подкислением и фосфатированием;
• возмещением потерь равновесной углекислоты в системе оборотного водоснабжения путем добавки в воду углекислоты дымовых газов (рекарбонизация);
• умягчением добавочной воды известью с осветлением натрий-катиониро — ванием или водород-катионированием с голодной регенерацией.
Кроме того, используют обработку оборотной воды магнитным полем, ультразвуком и др.
На этих способах можно не останавливаться, поскольку они хорошо известны В отечественной и зарубежной практике наибольшее распространение получили методы, описанные ниже.
Классификация применяемых сегодня методов стабилизационной обработки воды приведена в табл. 3.11.
Следует отметить, что препараты зарубежных фирм имеют рад недостатков при использовании в условиях отечественных месторовдений. Большинство их плохо совместимы с пластовыми водами, содержание солей в которых значительно выше, чем на месторождениях ряда зарубежных стран. Многие несовместимы с антифризами и, следовательно, не могут быть использованы в условиях низких температур. Не всегда составы композиции обладают универсальностью действия в отношении отложений смешанного состава. Одни ИС термически нестойки, другие увеличивают вынос механических примесей. Используемая концентрация зарубежных препаратов, как правило, достаточно высока и составляет 10—20 мг/дм , что вызывает неоправданно большие расходы реагентов. Применение препаратов зарубежных фирм не всегда экономически оправдано.
|
Таблица 3.11 МЕТОДЫ СТАБИЛИЗАЦИОННОЙ ОБРАБОТКИ ВОДЫ ПРИ JL> О
|
|
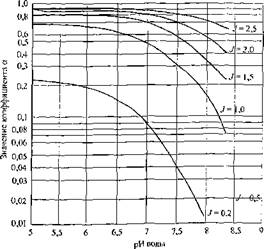
Рис. 3.5. График Д. ІЯ определения коэффициента б при стабилизационной обработке воды подкисле — иием (рН_ < рНо < 8,4) |
Дня решения задач нефтедобывающей и газодобывающей промышленности создан отечественный ассортимент эффективных ингибиторов солеотложения на основе фосфорсодфжащих комплексонов типа аминоалкилфосфоновых и алкилидендифосфоновых кислот.
Представляется вероятным, что наибольшим эффектом должны обладать соединения, сочетающие поверхностно-активные и комплексе образующие свойства.
Оценка эффективности действия комплексонов и композиций на их основе по предотвращению образования осадков солей СаСОэ, CaSOa, Ва80л осуществляется, как правило, одним из описанных ниже методов.
Изучение образования отложений солей непосредственно на поверхности металла в динамических условиях при повышенных температурах от 35 до 80 °С. Эффективность действия ингибиторов определяется массой образовавшегося отложения на поверхности металла.
Определение индукционного периода образования осадка, которое основано на определении времени с момента образования пересыщенной системы до выпадения осадка; оцениваемого по изменению интенсивности проходящего через раствор света или его электропроводности.
Сравнительная оценка эффективности реагентов — ингибиторов в статических условиях, основанная на их способности удерживать осадкообразующие катионы (Са", Ва *) в объеме раствора, препятствуя образованию осадков CaS04, CaC03, BaS04. Этот метод получил наиболее широкое распространение.
Влияние ряда комплексонов, содержащих как карбоксильные, так и фосфо — новые группы, на процесс кристаллизации сульфата кальция предс тавлено в табл. 3.12 и 3.13.
Добавки карбоксилсодержащих комплексонов (НТА, ДПА) практически не влияют на параметры зародышеобразования и кристаллизации сульфата кальция. Комплексоны, содержащие фосфоновые группы, способствуют увеличению удельной поверхностной энергаи зародыша, его радиуса, уменьшению скорости зародышеобразования. Значительно увеличивается индукционный период кристаллизации, при этом наблюдается корреляция продолжительностью периода индукции в присутствии комплексонов. Ингибирующий эффект возрастает с ростом числа фосфоновых групп в молекуле комплексоиа от ИДУМФ и ГФ к НТФ, с увеличением числа атомов азога (от ИДФ и НТФ к ЭДТФ, ДПФ, ДБТФ).
В рассмотренном ряду комплексоиов большой интерес представляет НТФ.
Он сочетает высокую эффективность предотвращения выпадения CaS04 с высокой термостойкостью (до 200 °С) и технологической доступностью.
Результаты изучения взаимодействия НТФ со щелочноземельными металлами и магнием позволили установить, что механизм ингибирования солеот-
|
Таблица 3.12 ВЛИЯНИЕ КОМПЛЕКСОНОВ НА ПАРАМЕТРЫ ЗАРОДЫШЕОБРАЗОВАНИЯ СУЛЬФАТА КАЛЬЦИЯ (при 40±0,1 °С)
|
|
Таблица 3.13 ВЛИЯНИЕ КОМПЛЕКСОНОВ НА КРИСТАЛЛИЗАЦИЮ СУЛЬФАТА КАЛЬЦИЯ ________________________ (с№„,”7,()г/л;7-=40±0,1»С) ___________
|
ложений довольно сложен. По-видимому, в сильноминерализованных пластовых водах происходит одновременное образование как водорастворимых комплексов CaHL"’1, BaHL"4, Mg HnL, vJ (pH = 3-6) или CaLT, BaL4, MgL4_(pH = = ?-10), так и малорастворимых полиядерных комплексов состава Ca5(HL)2, Ba5(HL)2 (pH — 5-6) и Ca3L, Ba3L (pH = 7-9). В последнем случае эффективность реагента о бус л ов л ивается, вероятно, замедлением роста кристаллов гипса, кальцита, карбонатов или сульфатов бария в результате блокирования граней их кристаллов малорастворимыми полиядерными комплексонатами.
Композиции на основе отходов производства НТФ наряду с высоким эффектом ингибирования отложения солей СаС03 и CaS04 эффективны и как ингибиторы образования осадков BaS04, значение pH их водных растворов равно 6-7, т. е. они некоррозионно-акпшны. Состав композиции на основе НТФ, включающий этиленгликоль, благодаря синергетическому эффекту действия компонентов позволяет уменьшить расход НТФ на 30-50 % и упростить техноло-
гию примешлм ингибитора за счет снижения температуры замерзания сое
ва до минус 30—минус 50 СС. ‘ №
Наиболее эффективен НТФ в сочетают с некоторыми полимерными спет,
«енити. Гак применение НТФ в смеси с полиакриловой кислотой
акржаышш, с сошлимфами акриловой я метшршювоГ, кислот с юй, винилсульфояовой, витлфосфоювои кислотам», иш. ташштГэГ
«umRii
виниловым эфиром позволило значительно повысить -эффективность ингибирования сожотожтш при одержании НТФ 0,1- № мг/дм’. Составы на основе НТФ и полиакриламида (ПАА) имеют улучшенные адсорбционно-десор — бдионние характеристики, например, предельная адсорбция НТФ на кварцевом песке, равна 0,2 мг/r, при добавке к ней 0,5 % и более ГІАА, адсорбция
увеличивается до 0,6 мг/г.
Эффективным ингибитором отложений солей CaS04 и СаСО, являет ОЭДФ. Влияние ОЭДФ на кристаллизацию СаС03 связано, вероятно, сорбцией ее на поверхности образующихся микрокристаллов. При этом увеличиваются и удельная поверхностная энергия и радиус критического чародыша (табл. 3.14).
Перспективно использование комплексонов для предупреждения отложений парафина в скважинах и нефтепромысловых трубопроводах. Весьма эффективным для этой цели является сочетание ДПФ-1 и силиката натрия. Образующаяся на стальных поверхностях защитная гидрофильная пленка прочно удер-
слом1й^и«
кшгаетаїТісе^ образовывать устойчивые растворимые в воде
сульфида желе™ п™ РеД°твращать тем самым возникновение осадка
и подготовку разносортных тгк~,П СОВмесп<>’10 Добычу, транспортировку
При добыче рйзносортных! дозировочного устройств Не(*пеи на забой скважины постоянно с помощью
виваленгном содержаще,! ®ДадтдинатРиевУ’о соль ЭДТА в количестве, эк-
комшіексоната железа ПШ ^ f 100-200 мг/дм5) для образования введенный в скважину комт ^Єрацию ос>’Ществляют таким образом, чтобы
%»*** смеш®ание желе™™ * Попадал в Нефть девонского горизонта. Пос-
о) нефтей не привода к 0кпяДерЖащей %) и сероводородсодержаи™
и, как следствие^ наблюдает-
ся повышение вязкости продукции скважины. Наибольшее распространение в отечественной и зарубежной практике для отмывки оборудования получили ЭДТА и ее соли.
Устойчивость комплексов, образуемых ЭДТД и ее солями, так высока, а концентрация свободного катиона, образуемого в результате диссоциации комплекса, настолько мала, что при этом не достигается произведение растворимости для большинства труднорастворимых соединеиий, прису тствующих в воде теплообменного и теплоэнергетического оборудования, это и обусловливает эффективность комплексона.
Универсальность ЭДТА проявляется в способности образовывать комплексы со всеми катионами, присутствующими в воде. Четырех валентные металлы образуют, как правило, наиболее устойчивые комплексонаты в растворах (pH < 1) трехвалентные — при pH = 2-3,5. Комплексонаты тяжелых двухвалентных металлов образуются при pH = 3,5-5, щелочноземельных — при pH = = 7-12 [233].
Термическое разложение ЭДТА и ее солей происходит в интервале 140-250 °С, причем устойчивость соли в сравнении с ЭДТА тем больше, чем больше степень замещения; термическое разложение комплексонатов Fe и Са происходит при температурах более высоких, чем разложение самого комплексона.
Для удаления кальциевых отложений на внутренних поверхностях конденсаторных трубок используют растворы трех-, четырехзамещенкых солей ЭДТА. Коррозия латунных трубок в растворе комплексона незначительна, тем более что связывание кислорода в растворе гидразингидратом уменьшает скорость коррозии латуни приблизительно в 10 раз.
К настоящему времени накоплен большой положительный опыт использования раствора комплексона для очистки котлов от железооксидных отложений. В качестве комплексона может быть использован раствор двух-, ірехза — мещенной соли ЭДТА.
Однако при этом необходимо введение дополнительного кислотного агента Для создания в отмывочном растворе низких значений pH, необходимых для комплексования железа.
Использование раствора натриевых солей ЭДТА возможно только для очистки от оксидных отложений железа (III), применение двузамещениой аммонийной соли ЭДТА позволяет растворять и оксиды железа (III), так как при повышении температуры раствора введенная в систему термически неустойчивая днаммоцийная соль превращается в ЭДТА, значение pH раствора понижается, что делает возможным комплексование Fe3+. Создание концентрированного раствора ЭДТА непосредственно ее растворением затруднено из-за ограниченной растворимости кислоты в воде.
Локальные сооружения с растворами комплексонов разработаны для прямоточных котлов сверхкритических параметров, работающих на мазуте. Для
обеспечения достаточной эффективности очистки растворами ЭДТА и ее солей скорость движения расгвора должна быть в пределах 1,5-2 м/с. Локальную очистку без ингибиторов коррозии проводят при 150-180 °С. Концентрация солей ЭДГА в растворе 0,4-0,5 г/кг, значение pH от 5-6 (двузамещенная ссшь) до 8-9 (трехзамещепная соль).
В связи с тем, что для взаимодействия ЭДТА и ее солей с разными катионами оптимальные значения pH различны, универсального действия этого комплексона трудно достичь. Разработаны композиции на основе ЭДТА (с концентрацией компонентов 10 г/дм3, для растворения железооксидных отложений в которых необходимое значение pH создается добавками органических кислот (лимонной, щавелевой, янтарной, гяутаровой, адипиновой), а также малеино — вого и фталевого ангчдрвдов. Органическая кислота более активно переводит железо в раствор в виде комплекса невысокой устойчивости, который в результате смешанного камплексообразования с ЭДТА переходит в разнолиган — дный комплекс высокой устойчивости, Введение в композицию восстановителей (гидразина, фенилгидразина) вызывает образование ионов Fe21, ускоряющих процесс растворения гематита Fe203 в растворе динатриевой соли ЭДТА.
Композиции на основе натриевых солей ЭДТА применимы, прежде всего, для предпусковых и эксплуатационных химических очисток котлов сверхкри — тнческих параметров. Они моїуг использоваться и для очистки поверхностей любых конструкционных материалов, в том числе аустенитиых нержавеющих сталей. Впервые эти композиции были применены на Троицкой Г РЭС.
Одной из важных задач теплоэнергетики является растворение отложений на основе карбоната кальция. Для этой цели весьма эффективны фосфорсодержащие комплексоны. Являясь достаточно сильными кислотами, они обладают высокой растворяющей способностью по отношению к СаСО.,. Так, ОЭДФ и ее аналоги предложено использовать для удаления молочного н пивного камня, накипи в теплообменниках, трубопроводах и охлаждающих системах, в системах питания бойлеров.
В последние годы для предотвращения образования минеральных отложе — ний в системах отопления, охлавдения и других оборотных циклах широкое распространение в России получили относящиеся к классу комплексонов орга — нофосфонаты (ОФ) н композиции на их основе. По сравнению с химическим или ионообменным обессоливанием оборотных вод, применение ОФ требует существенно меньших затрат, поскольку практически полное предотвращение минеральных отложений достигается при низких расходах ингибитора в интервале 1-5 г/м5. Простота применения, при существенном сокращении капитальных вложений и эксплуатационных расходов, обуславливает популяр’ ность химических методов ингибирования минеральных отложений.
Если не учитывается химическая природа ингибиторов, механизм их взаимодействия с компонентами растворов, кинетические и термодинамические
параметры реагентов, применение ОФ не дает ожидаемых результатов или даже приводит к отрицательным последствиям. Сложность выбора необходимою реагента связана, в частности, с большим количеством предложений со стороны отечественных и зарубежных фирм, которые зачастую носят коммерческий характер и не позволяют провести сравнительную оценку их эффективности.
Выяснение механизма образования минеральных отложений и влияния на этот процесс ОФ, по нашему мнению будет способствовать осознанному выбору реагентов и оптимизации условий их применения.
Образование минеральных отложений является, следствием кристаллизации солей из пересыщенных растворов. Термическое разложение солей временной жесткости приводит к образованию пересыщенных растворов малорастворимых карбонатов кальция и магния, а термодинамические нарушения равновесия в пересыщенных растворах солей постоянной жесткости вызывают кристаллизацию сульфатов, фосфатов, оксалатов и других малорастворимых солей кальция, стронция, бария. Согласно современным воззрениям, пересыщенный раствор представляет собой ультрамикрогетерогенную систему (промежуточное состояние между истинным и коллоидным растворами), в объеме которой непрерывно происходит образование и распад микрозародышей кристаллической фазы. Двнжушей силой их образования является величина пересыщения, определяемая как разность между текущей и равновесной концентрацией.
Ультрамикрозародыши термодинамически неустойчивы и, при определенных условиях, играют роль центров кристаллизации, продолжая свой рост. Важнейшими условиями, оказывающими влияние на образование и рост центров кристаллизации, являются температура, pH среды, наличие в воде солей и малорастворимых примесей, гидродинамика и физико-химическая природа подложки. Обобщенную схему образования кристаллов из пересыщенных растворов можно представить следующим образом:
ионы о молекулы ассоциаты о ультрамикрозародыши «-»■ зародыши кри
тического размера <-> кристаллы твердой фазы.
Образование зародышей критического размера происходит в течение периода индукции и не может быть определено аналитическими методами из-за малого значения массовой доли образующейся твердой фазы. Работа образования критического зародыша (s) и порядок реакции зародышеобразования (п) могут быть рассчитаны по продолжительности индукционного периода (f. nd) из уравнения Гиббса — Фольмера и модели Христиансена — Нильсена соответственно:
6кN, c3M2 1
ln2(c/c ) <ЗЛ5)
где А — постоянная, зависящая от принятого масштаба процесса; JV Авокадо; М— молярная масса кристаллизующегося вещества; R 1. Число зародыша критического размера; Ти р—температура и плотность раств8^0 и ср—текущая и равновесная концентрации; к—константа скорости ре °^°’с зародышеобразования. кЧиа
|
t. /=к, |
Из данных, представленных в табл. 3.15 видно, что с уменьшением Da римости увеличивается работа по образованию зародыша критического Тб°~ мера и уменьшается порядок реакции зародышеобразования. Т. е. чисд0 ^аз~ лекул, необходимых для образования критического зародыша. Это спиде ^ ствует об относительной устойчивости пересыщенных растворов Maji0paTeJlb~ римых солей в стационарных условиях. На практике, влияние перечислен 6°~ выше внешних воздействий сказывается в ускорении процесса кристал„ ^ ции. а~
Устойчивость коллоидных растворов определяется электростатичес стабилизацией, обусловленной величиной заряда коллоидной частицЬ)_ бипьность коллоидных растворов связана с гидрофилизацией поверХн мицелл, зависящей от тмщины двойного электрического СЛОЯ, уменьще Т<і которого при снижении величины заряда приводит к флокуляции и коагу 46 ции коллоидных частиц, Аналогично, снижение степени гидрофил изации те64′ дой фазы приводит к ее росту и укрупнению кристаллов.
Установлено, что незначительные добавки ОФ практически не оказьіва влияния на активность ионов в растворе и не препятствуют эндотермичеС({ т му процессу образования зародышей в индукционный период.
В то же время, в присутствии ОФ возрастают основные параметр зародышеобразования малорастворимых солей sun, что приводит к Уменьц^1 нию вероятности образования кристаллической фазы, поэтому их влия^’ может быть объяснено взаимодействием полярных групп ОФ с зародыц1а^е
|
Таблица 3 ^ ПАРАМЕТРЫ ЗАРОДЫШЕОБРАЗОВАНИЯ КРИСТАЛЛОВ 5 МАЛОРАСТВОРИМЫХ СШЕЙ ПРИ 313К
|
кристаллизирующейся соли и образованием на границе раздела фаз стабилизирующих сольватных слоев.
Образование таких слоев возможно при выполнении ряда требований, которым, должны удовлетворять реагенты, используемые для этих целей
• наличие поверхностно активных свойств по отношению к і-ранице раздела между дисперсионной средой и твердой фазой,
• склонность к образованию с катионами металла, входящего в состав кристаллов, внутрикомплексных соединений;
• взаимодействие между реагентом и частицей, подлежащей стабилизации, должно быть оі-раничено образованием поверхностных химических связей;
• образование сольватных слоев на поверхности должно происходить одновременно с появлением частиц твердой фазы.
ОФ в полной мере соответствуют указанным требованиям. Величина адсорбции на кристаллизующейся твердой фазе невелика и составляет около 0,2 мг/ г. ОФ, как представители класса фосфорсодержащих комплексонов, образуют устойчивые комплексы с ионами щелочноземельных металлов с рК = 3—7. Устойчивость карбоксилсодержащих комплексов щелочноземельных металлов значительна выше (рК > 10), однако они не обладакгг свойствами стабилизации пересыщенных растворов, т. к. образуют соединения стехиометрического состава, не содержащие свободных функциональных групп. Адсорбционные слои для них являются неустойчивыми и десорбируются.
Механизм стабилизирующего действия ОФ, по нашему мнению, заключается в адсорбции на активных центрах зародышей кристаллизующейся соли. Число таких центров невелико, и располагаются они, по-видимому, на гранях и ребрах растущих кристаллов. В таком взаимодействии участвуют только атомы и ионы, принадлежащие кристаллической решетке и находящиеся в поверхностном слое кристалла. Результатом этого взаимодействия является гид — рофшшзация поверхности, в результате чего рост кристалла прекращается, и, как следствие, отложения не образуются. Добавки ОФ в пересыщенные растворы резко уменьшают вероятность образования зародышей критического размера и, тем самым, уменьшают (или сводят к нулю) скорость роста кристаллов.
Собственно, Этим и объясняется малый расход ОФ (1-5 г/м3) при котором происходит предогвращение солеотложений. Исходя из средних размеров молекул ОФ, примем площадь, занимаемую одной молекулой 10-19м~(10-1 нм"). Тогда в кубометре раствора при концентрации ОФ 3 г/м’ (или 102 моль/м3 при средней молекулярной массе ОФ 300 г/мсшь), с учетом значения числа Аво — гадро N А, будет занято около 6-102 м2 поверхности кристаллизующейся фазы. Определенная нами методом адсорбции азота удельная поверхность кристаллизирующегося сульфата кальция составляет 3 м2/г. При содержании в 1 м3 раствора твердой фазы массой 3 кг общая поверхность кристаллов составляет
9-Ю3 м2. Таким образом, ингибирование солеотложений происходит, когда ОФ покрывает около 7 % поверхности кристаллической фазы. Это подтверждает тезис о том, что взаимодействие ОФ происходит лишь с активными точками на гранях и ребрах растущих кристаллов, и объясняет малый расход реагента, необходимый для стабилизации.
Если концентрация ингибитора солеотложений недостаточна, чтобы подавить процессы образования зародышей критического размера, то происходит кристаллизация полидисперсной фазы. При этом средние размеры образующихся кристаллов превышают те, что образуются без ингибитора. В присутствии ОФ кристаллы не образует прочных отложений на стенках трубопроводов, что позволяет периодически удалять образовавшийся осадок из оборотной системы, например, продувкой.
Использование больших концентраций ингибитора экономически не оправдано. Кроме того, при больших концентрациях ОФ в обрабатываемых растворах происходит образование комплексов, близких по составу к стехиометрическому. В этом случае эффект ингибирования может уменьшиться или вообще исчезнуть, поскольку фосфоновые группы, которые при оптимальных концентрациях взаимодействуют с поверхностью кристаллической фазы и препятствуют росту зародышей, при больших концентрациях участвуют в образовании полидентатных связей с катионами металлов, вплоть до перезарядки поверхности кристаллов.
Отечественной промышленностью налажен выпуск ряда ингибиторов на основе ОФ. Одним из наиболее эффективных среди них является реагент, известный под торговой маркой «ИОМС» (ингибитор отложений минеральных солей). Разработаны достаточно простые технологии, позволяющие модифицировать ИОМС, придавая ему специфические, в том числе биоцидные и антикоррозионные, свойства (А. С. 726123 СССР, Б. И. 1980, № 3; патент России № 2065410, Б. И., 1996, № 23; патент России № 2133229, Б. И., 1999, № 20; патент России № 2133751, Б. И., 1999, № 21).
Для борьбы с биоотложениями и коррозией служат ОФ, модифицированные соединениями меди (II) и цинка. Катионы меди цинка образуют с ОФ мо — ноядерные комплексы, константы устойчивости которых соответствует интер„ валу рК от 12 до 20. Эффективное ингибирование коррозии, соле — и биосппо, жений наблюдается, когда массовая доля медь-цинк-содержаших комплексо. нов составляют около 20 % от общей массы используемых ОФ.
В настоящее время на Северском трубном заводе (г. Полевской, Свердлове, кой обл.) осуществляется внедрение стабилизационной обработки воды от, ытых оборотных циклов, в которых велика вероятность образования сод6, отложений и биологического обрастания. Для этой цели используется комп0. зиция ИОМС и его медного комплекса. Комплексные ингибиторы, предназна, иные для обработки воды в паровых котельных с целью предотвращение
солеотложений, кислородной и электрохимической коррозии, были испытаны и внедрены на Екатеринбургском заводе «Pepsi». Замена импортного аналога «Кіпріех 180» (США) ингибитором на базе ИОМС позволила в 3-4 раза сократить затраты на водопсщготовку.
Интерес представляет использование ОФ на предприятиях большой и малой энергетики, занимающихся производством горячей ВОДЫ, электрической и тепловой энергии. Замена технологий водоподготовки с использованием, например, Na-катионирования на технологии химической обработки воды с применением ОФ сокращает потребление воды на регенерацию фильтров и эксплуатационные затраты на обслуживание оборудования традиционной водоподготовки. Методы химической обработки воды с применением ИОМС испытаны и внедрены на десятках котельных различных предприятий Свердловской, Челябинской, Магаданской и др. областей. На практике отмечена высокая стабилизирующая способность ингибиторов группы ИОМС. используемых в системах питання водогрейных котлов различных типов при карбонатном индексе до 21 и темпераіурах на выходе из котаа до 140 °С.
В результате внедрения технологий химической обработки воды оборотных циклов обеспечивается экономия энергоресурсов, сокращаются объемы ремонтных работ, реализуется переход на схемы бессточного водопользования без крупных капиталовложений, сокращается неблагоприятное воздействие на окружающую природную среду и снижаются затраты на приобретение дорогостоящих (часто импортных) реагентов.
Интересные результаты были получены но предупреждению образования отложений солей жесткости на поверхностях нагрева, теплообменного оборудования с использованием антинакипина СК-110. который выпускается по ТУ —245830-33912561 -97, не содержит вредных примесей, ПДК в воде — 3,5 мг/ ДМ‘ согласно ГН 2.1.15.963а-00- Внедряется в соответствии с «Технологическим регламентом на технологию применения реагента СК-110 в системах теплоснабжения и горячего водоснабжения населенных мест и промышленных предприятий», согласовано с Минэнерго РФ, Минэкономики РФ. Госгортехнадзором РФ.
Антинакипин СК-110 широко используется в системах водяного охлаждения оборудования (доменные, электроплавильные и мартовские печи, конвертеры, ТЭЦ, ТЭЦ-ПВС, MHJ13, кислородные и компрессорные станции, коксохимическое производство и т. д.)
Расход реагента 6-21 мг/дм3 (по товарному продукту) в расчете на подпиточ — ную воду.
Обработка воды антинакипипном СК-110 позволяет полностью исключить образование отложений в сетях и на оборудовании, в результате чего:
• повышается надежность и экономичность работы основного технологического оборудования;
• полностью или частично прекращается сброс сточных вод в природній водоемы, сокращается потребление свежей воды;
• увеличивается срок службы межремонтные периоды работы оборудовЗ’ ния;
• исключаются Химические очистки оборудования и сброс химзагрязненнЫ* стоков;
• исключаются трудоемкие операции, улучшаются условия труда обслужи’ вающего персонала. Кроме этого антинакипин используется в системах обо’ ротного водоснабжения загрязненных вод (газоочистки доменных и ферросплавных печей, разливочные машины, агпопроизводства, системы ГЗУ ТЭ11 и т. д.). Рекомендуется для использования в системах, вода которых характерй’ зуется высоким содержанием солей жесткости и высокой щелочностью. Соли из производства покупают в воду непрерывно, и их необходимо выводить из системы. Исходя из этого, ангинакипин вводится в воду перед сооружениями, которые необходимо защитить от отложении, т. е. перед газоочистками и градирнями. Соли в виде карбонатов выпадают в отстойниках и удаляются со шламом. Расход реагента составляет 4-10 мг/дм3 в расчете на всю оборотную
|
Водолхпаждаемое оборудование
антинашшна |
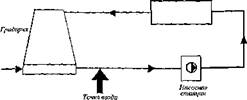
Рис. 3.6.
|
Дилччпшя Газоочисітюй Раоиачышй Насосная Виппншмсрноя печь аппарат отстойник станция гирдирих |
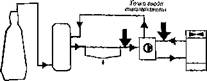
Рис. 3.7.
воду. Скорость образования отложений в сетях, на сооружениях н оборудовании снижается в сотой раз, за счет чего удается:
• повысить надежность работы газоочистных аппаратов;
• увеличить срок службы оборудования и продолжительность межремонтных периодов;
• исключить продувки и аварийные сбросы воды из системы, сократить потребление свежей воды;
• улучшить очистку и охлаждение доменного газа;
• снизить расход электроэнергии на перекачивание воды.
Выбор того или иного способа обработки воды определяется главным образом качеством воды и условиями ее использования. Ориентировочно способ обработки охлаждающей воды в системах оборотного водоснабжения при нагреве ее до 40-60 °С и охлаждении на градирнях или в брызгальных бассейнах, в зависимости от величины карбонатной жесткости воды (не загрязненной поверхностно-активными веществами), можно принимать по табл. 3.16. составленной на основании многочисленных исследований на модели и практики эксплуатации.
Наиболее надежным будет исследование, как термостабильности каждой воды, так и методов ее обработки с учетом конкретных условий.
Термостабильность воды и эффективность ее обработки тем или иным методом для предотвращения образования карбонатных отложений исследуются в натурных условиях и на модели. В том и другом случае критерием могут быть изменения качества воды по коэффициентам концентрирования отдельных ионов или их суммы (общее солесодержание) и величина скорости отложения карбонатов.
Коэффициент концентрирования. В открытой системе оборотного водоснабжения (с охладителем) происходят потери воды, вызываемые испарением части ее в охладителе и уносом мелких капель воздухом, выходящим из охладителя (градирни, брызгального бассейна). Испарением теряется в среднем около 0,15% охлаждаемой воды при понижении температуры на 1 %, уносится воздухом в градирнях 0,2-0,3 % охлаждаемой воды.
В аппаратах прямого контакта (барометрические или струйные конденсаторы, трубы Вентури и скруббера для очистки газов) вода дополнительно теряется в виде пара через дымовую трубу в атмосферу; в других случаях конденсирующийся водяной пар служит скрытой добавкой воды в систему.
Считается, что растворенные соли испарившейся воды (полностью или частично) остаются в оборотной воде, повышая их концентрацию. Все потери воды в охладительной системе оборотного водоснабжения компенсируются добавлением воды из источника. Кроме того, обычно оборотная вода освежается продувкой, что снижает общее солесодержание и концентрацию отдельных ионов. В результате воздействия всех этих факторов иногда достигается
|
Подкислеиие добавочной воды и фосфагоровзние оборотной воды (совместная обработка) Умягчение добавочной воды известью с осветлением Умягчение части или всей добавочной воды Ыа или Н- катиониробанием с голодной регенерации |
|
шит Пвдотвтщннвд отшов^ЕЙ ВОДЫ (ОРтнт,1РОвтт Ш в СИСТЕМАХ ^ КАРБОНАТНЫХ ОТЛОЖЕНИЙ ДО 40-65 °С И П№ »ЛГгаВЕ ВОДЫ |
|
С ИЛИ В БРЫЗГАЛЬНЫХ |
|
Карбонатная жесткость (щелсм- ИОСТЬ) природной ЕОДЫВ МГ-Э1ГВ/ПМ3 |
|
|
реки, водохрам/- лпща средней |
подземные ис |
|
ПОНОСЫ |
точники |
|
<2,5 |
<1,5 |
|
2,5-4 |
< 1,5-3 ] |
|
2,5-5 |
1,5-5 |
|
4-6 |
3-5 |
|
>4-5 |
|
|
>4-5 |
|
Подкислеиие добавочной воды Рекарбонизация оборотной воды |
При наличии дымовых газов, содержащих СОг* и невысоком коішенгрирошшии (упаривании)
При условии ограничении концентрации SCV При наличии дымовых газов и невысоком концентрировании.
Если вода и без того нужд»ст-
ся в осветлении
если вода не нуждается
предварительном осііСТ
. и м с ч d її и я. и для боды рек и водохранилищ северных районов, а также с »^пч г. эКБ/лм. питанием указанную в таблице карбонатную жесткость (щелочность) следует повысить на м в
2. При нагреве воды в проиэводстне ниже 40 °С температурным перепадом? / ? 5®, Ре^?ме1пРДКцслс’ таблице величина карбонатной жесткости может быть увеличена на 0,5-1 мГ-экв/дм . 3. ^ионов с и иии добавочной поды необходимо считаться с тем, чтобы в оборотной воде содор^|^е2 * вопы SCV было не более соответственно 350 и 600 мг/дм3, а общая щелочность (НСО + СО* J’ £ОНаТцоЙ была не менее 2 мг-экв/дм3 во избежание развития коррозионных процессов. (На снижение г по_ жесткости воды на 1 мг-экв/дм3 расходуется 49 Vfffjsbv МКУ/о-ноЙ серной иисяоты, при 3X0,1 ступают ионы S042′ в количестве48 мг/дм3).
своего рода равновесие, при котором устанавливающиеся к0ИцентрацИ”о^,1 и сят от соотношения между поступающим и удаляемым количеством
растворенных веществ. петучих я ие
Степень повышения концентрации растворенных веществ (не ле у ^ф_ образующие осадка) называют коэффициентом ‘можех быгь
фициентом упаривания. Численное значение этого коэффициент
выражено так:
|
|
|
а) по упариванию воды |
(3.17)
6) по концентрированию солей
|
(3.18) |
Ліб ■ ^лоб или Ка ~ (‘1,6 ■ Сідоб »
me fViim — потери воды из системы на испарение; IV — потери воды из системы уносом; И1′ сброс воды из системы для освежения (продувка); Рл, РтГ> — концентрация растворенных в оборотной и добавочной воде солей;
С1 а1 С1ис — то же, хлоридного иона.
В практике дня контроля в системах оборотного водоснабжения используется обычно коэффициент концентрирования хлоридного иона (при условии, что вода не хлорируется) Ка = СІ о5:СГа і6, величина которого сравнивается с коэффициентами концентрирования карбонатной жесткос ти Кжк=Жі. Ф:Жіізі! Б, кальция КГа = Са‘’п(.:Са"!1лЛ или других ионов. При хлорировании воды вместо хлоридного иона С1 концентрирование контролируется по иону магния Mg2*.
В действующих охладительных системах оборотного водоснабжения с градирнями коэффициент концентрации может изменяться в широких пределах, но во многих случаях он составляет летом 2 и зимой 1,5. С увеличением количества сбрасываемой (и добавляемой в систему) воды коэффициент концентрирования падает, одновременно снижается и коэффициент использования воды.
Сравнивая величины коэффициентов концентрирования хлоридного иона, карбонатной жесткости или, других веществ, полученные по воде и вычисленные по данным аналитического определения, можно получить представление о поступлении новых веществ и о выпадении их в осадок (отложения), т. е. о термостабилыюсти воды.
В качестве примера на рис. 46 показаны результаты исследования изменения качества воды в системе оборотного водоснабжения пиролиза газа ка одном из химических комбинатов. Продукт — подсмольная вода — оборотной водой в оросительном холодильнике. В систему добавлялось такое количество воды, которое лишь компенсировало ее потери на испарение и унос (без сброса). Коэффициенты концентрации вначале были равными КС1 = СГ^: СГдо6 = 85:41 ~ 2 и = Жка = 3,6:1,8 = 2; затем установилось их неравенство > Кш. Вода была не термостабильной, при этом на омываемой охлаждающей водой поверхности труб оросительного холодильника наблюдалось интенсивное образование карбонатных отложений, которые за период работы между ремонтами (11,5 мес.) достигали 10-15 мм.
Этот метод контроля неприменим при прямом контакте водм с продукт0’1’’а гакже при хлорировании оборотной воды.
Скорое, пь отложении. Данные химического анализа воды и величина коэффициента концентрирования не дают еще представления о ее термостабипь — носщ. Целесообразно вести контроль за скоростью отложений. Ввиду труД*’ сги его осуществления непосредственно натепяопередающей поверхности Алї! практических целей придается ограничиваться установлением относительной скорости отложений на индикаторных пластинках (стеклянных «ловчих» или стальных).
По разнице в весе пластинок (при условии, что одновременно не происходит коррозни металла), экспонируемых в исследуемой воде (с отложениями и без них) и высушенных до воздушно-сухого состояния в течение примерно 48 ч, определяется общая скорость сггясмсений (аналогично биологическим обрастаниям). После химического анализа этих отложений и определения содержания в них кальция вычисляется скорость собственно карбонатных отложений.
Скорость отложений будет:
весовая
„ Мг — М.
С0 =—— г/(м — ч); (3.19)
С
ha = 0,73-—^ мм/мес., (3.20)
где Мх и М2 вес пластинки до и после экспозиции (с отложениями), г; F площадь поверхности пластики (со всех сторон), м2;Т — продолжигедь ность экспозиции пластинки, ч; 0,73 ~ жоэффишент пересчета; р„ — плот! ноегь (объемный вес) карбонатных отложений, г/см3.
При отсутствии данных исследования можно принимать р равным (в г/см3}, для рыхлых карбонатных отложений с биологическими обрастаниями 1,4—2,55 (среднее 1,5), для плотных карбонатных отложений 2,12-2,54 (среднее 2,28^ для железистых карбонатных отложений 3.
Результаты вычислений заносятся в журнал, затем находится среднее значе, ние скорости отложений С и йо для всех пластинок. Сравнение полученные результатов со скоростью отложений (табл. 3.17), составленных многочислен, ньши опытами, позволяет отнести исследуемую веду к той или иной группе термостабильности и решит* вопрос о целесообразности освежения оборот, ной воды или ее обработки тем или иным методом.
|
Т аб л и ца 3.17 ШКАЛА ТЕРМОСТАБИЛЬНОС’ГИ ОХЛАЖДАЮЩЕЙ ВОДЫ
|
При исследовании скорости отложений в натурных условиях индикаторные пластинки, собранные в кассету устанавливаются в поток воды за теплообменным аппаратом (в конце его или в трубопроводе). При исследовании на модели пластинки устанавливаются в закрытой специальной кассете.
В заключении не можем не упомянуть об еще одном новом направлении, которое уже находит применение в практике работы с водой.
В настоящее время одной из новых и интенсивно развивающихся технологий водоподготовки является энергоинформационная обработка воды на основе комплекса физических воздействий (гидравлического удара, кавитации, резонансных молекулярных и ультразвуковых колебаний, импульсных электрических разрядов, электромагнитных излучений и др.).
Как следует из ряда докладов, опубликованных в трудах международного коніресса «Вода. Экология. Технология — ЭКВАТЭК-2004», подобная обработка, изменяя некоторые физические свойства воды (поверхностное натяжение, электропроводность, вязкость, pH, молекулярную структуру); придавая молекулам воды строго определенные молекулярные колебания, которые передаются потоком воды на дальние расстояния и сохраняются длительное время; интерферируя с колебаниями молекул и атомов загрязняющих веществ, приводит к возникновению в водных растворах как окислителъно-восстано — вительных реакций с участием соединений металлов и органических соединений, так и солюбилизации (переводу в коллоидную форму) труднорастворимых карбонатных, сульфатных, фосфатных отложений кальция, магния и оксидов железа.
Учитывая данные физико-химические механизмы, можно полагать, что энергоинформационная водообработка является весьма перспективным, без — реагентным, малоэнергоемким и эффективным методом очистки, обеззараживания, кондиционирования воды, а также борьбы с осадкообразованием, коррозией и биообрастанием контактирующих с водными растворами поверхностей.
Сама идея данного метода зародилась в России и первые научные исследования эиерго-информациоиных технологий были проведены учеными в 80- 90-х годах XX века в Ленинграде и Свердловске. Однако разработанные на этой основе приборы, которые сейчас наиболее активно исследуются и применяются, относятся преимущественно к медицинской практике и имеют малую производительность по обрабатываемой жидкости. К такого рода приборам относятся, например, «Ренорм», «Айрес» (Россия), «Гранде» (Австрия), «Антикальций» (Словения).
Одним из наиболее удачных примеров аппаратурного оформления этого метода для индустриального применения являются приборы — кольцо MERUS, производимые фирмой «MERUS» (Германия). Производительность приборов по обрабатываемой воде составляет от 10 до 32 ООО куб. м/сут. Прибор работает без контакта с водой. Не требует дополнительных источников питания, компактен, легко монтируется и не нуждается в обслуживании. Внешний вид прибора и схема его установки на трубопроводе показаны на рис. 3.8.
Опыт десятилетней эксплуатации прибора в 80 странах мира, в том числе и в России показал его высокую эффективность при использовании в системах отопления и водоснабжения коттеджей, отелей, в офисных и промышленных зданиях, градирнях, бассейнах, фонтанах и другом оборудовании для защиты новых стальных труб от коррозии. В результате работы прибора все оборудование (трубы, котлы, бойлеры и т. д.) независимо от вида и толщины отложений очищается до металлической поверхности, постепенно покрывающейся защитной пленкой насыщенного оксида железа (Fe304). При правильном подборе места установки прибора и отсутствии внешних электромагнитных полей действие прибора в трубопроводах начинается непосредственно с момента установки прибора и распространяется на расстояние не менее 10 км по течению воды.
Еще один пример — использование аквадиска, прибора, ие имеющего аналогов и выпускающегося в двух модификациях (500 и 2000). В основе работы
|
Рис 3 8 Внешний вид прибора и схема его установки на трубопроводе |
аквадиска лежит способ передачи и записи энергоинформационных потоков на вещество или комбинацию веществ (патенты Л» 2192902, № 2182122).
АКВАДИСК-2000 препятствует возникновению циан и сине-зеленых водорослей. Вода в водоемах дольше не зацветает и не загнивает. Он же не только останавливает отложение различных фракций на внутренних стенках емкостей, но и производит очистку от уже накопившихся. Например, Способствует отслоению ржавчины от внутренней поверхности емкости.