 Основные уравнения гидростатики и газовой статики
Основные уравнения гидростатики и газовой статики
Основное уравнение гидростатики:
Р=Р0 + рёИ, (5.19)
где Р — абсолютное статическое давление, Па; Р0 — внешнее статическое давление, Па; И — глубина, измеряемая по вертикали, м.
Следствием основного уравнения гидростатики является закон Паскаля: внешнее давление передается во все точки жидкости без изменения.
|
|
|
|
|
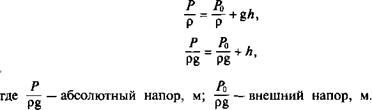
|
|
(5.22)
где р = р(Р)— уравнение вида термодинамического процесса изменения состояния жидкости (газа).
Экспериментально доказано, что основные параметры состояния реального газа (Р, Т, р, У^, V) приближенно связаны между собой в любом термодинамическом процессе в данный момент времени уравнением состояния совершенного (идеального) газа (уравнением Клапейрона — Менделеева) (5.23) — (5.26).
Совершенным называют газ (смесь газов), подчиняющийся уравнению состояния.
Чем меньше плотность реального газа, тем меньше его поведение отличается от поведения совершенного газа. При этом справедливы следующие зависимости:
|
|
||
где Л —удельная газовая постоянная, Дж/(кг • К); т — масса газа, кг; цм — молярная масса газа, кг/кмоль; для воздуха цм = 28,97 кг/кмоль;
= Ь — — молярный объем газа, м3/кмоль; при нормальных (физи-
ческих) условиях (Р= 101 325 Па, Т= 273,15 К) для любого совершенного газа цм = 22,41410 м3/кмоль; цмЛ — универсальная газовая постоянная, ц. мЯ = 8314,51 ДжДкмоль • К):
|
(5.27) |
![]() 8314,51
8314,51
Им Им
1 Iсмоль (киломоль) — условная единица количества вещества, содержит количество частиц, равное числу Авогадро (6,022 • 1026 кмоль1).
Количество вещества равно 1 кмоль, если число килограммов вещества равно относительной молекулярной массе:
цм = Mr ■ 1 кг/кмоль, (5.28)
где Mr — относительная молекулярная масса.
Мг = ‘^(пЗТ1АГ1), (5.29)
/ = |
где яат — число атомов в молекуле химического элемента; Аг — относительная атомная масса химического элемента; у — количество химических элементов в соединении.
Единицей количества вещества в СИ является 1 моль, однако удобнее пользоваться в расчетах величинами, в которые входит кмоль.
Связь между начальными и конечными значениями параметров состояния в изохорном (р = const, или г) = const), изобарном (Р= const) и изотермном (Г= const) термодинамических процессах определяет объединенный газовый закон:
= Д = const. (5.30)
-*/ Рм/
Процесс изменения состояния газа по глубине примем изотерм- ным. Решая совместно (5.22) и (5.30) после интегрирования, получим основное уравнение газовой статики:
Р = Р, е^, (5.31)
где е ~ 2,72 — основание натуральных логарифмов.
Или
P = Po^F, (5-32)
В уравнениях (5.19), (5.31) и (5.32) при рассмотрении статики жидкости (газа) в буровой скважине следует учитывать возможный наклон скважины:
h = L cos 0, (5.33)
где L — длина ствола скважины, м; 0 — среднее по длине скважины значение зенитного угла.
Разница между абсолютным и внешним давлениями жидкости называют весовым давлением Рв,
P-P0 = PB = pgh, (5.34)
Р Р — Р
— = ——— (5 35)
pg pg ’
Рв
где — — весовой напор жидкости, м.
При Р0 = Ра (сосуд открыт, жидкость граничит с атмосферой) Р„ = Ря. Разницу между абсолютным и атмосферным давлениями называют избыточным (манометрическим, сверхатмосферным) давлением Р„ и измеряют манометром.
Р-Р^Р«, (5.36)
Р Р — Р
— = ——— (5 37)
pg РВ ’ 1 ‘
где — избыточный (манометрический, сверхатмосферный) напор, м.
Разницу между атмосферным и абсолютным давлениями называют вакуумметрическим давлением Ртк и измеряют вакуумметром.
Рл-Р=Рт (5-38)
Р Р — Р
юк а (5.39)
pg Pg
* на
где —— вакуумметрическии напор, м.
г О
Определим максимальное значение высоты всасывания (вакуум- метрического напора) воды насосом в атмосферных условиях; при всасывании в камере насоса Р>РНП. Примем Р=РНП. При / = 4°С Ра = 0,981 • 105 Па, р = 1000 кг/м3, РИП ~ 0. Тогда (5.39) примет вид:
Рык „ Р,-Р Рш — о 0,981 -105 1П