 Получение кислорода из надперекиси натрия или калия
Получение кислорода из надперекиси натрия или калия
Надперекиси натрия и калия (общая формула Ме02) представляют собой твердые кристаллические вещества ярко-желтого цвета. Оии широко известны как эффективные средства регенерации воздуха в различных системах жизнеобеспечения. Их действие основано на чрезвычайно высокой активности к воде и водяному пару в широком интервале температур. Так как производимые продукты содержат незначительные примеси в виде окислов металлов, то по
лучаемый кислород не загрязняется примесями и не требует дополнительной очистки.
Надперекиси натрия и калия устойчивы при хранении в герметичной таре и начинают разлагаться при температурах выше 100 °С.
Получение кислорода при взаимодействии с водой идет согласно двум основным уравнениям реакции:
2Ме02+2Н20^2Ме0Н4-02+Н202+(?,. (8.9)
H2<WHj0-H/a02+<7j. (8.10)
Реакция (8.10) при нормальной температуре идет в течение нескольких часов. Однако, введя в массу надперекиси катализаторы разложения перекиси водорода, скорость реакции можно увеличить в десятки раз.
 Выход кислорода при гидролизе надперекиси натрия составляет 43,6%, надперекиси калия 33,2%. Общая теплота реакции гидролиза для надперекиси натрия 66,5, для надперекиси калия 55,2 кДж/моль. Реакция идет до конца при 5—7-кратном избытке воды. Поэтому наиболее перспективно использование иадпе — рекисей там, где нет больших ограничений по тепловыделению и использованию воды, например в энергоустановках морского назначения.
Выход кислорода при гидролизе надперекиси натрия составляет 43,6%, надперекиси калия 33,2%. Общая теплота реакции гидролиза для надперекиси натрия 66,5, для надперекиси калия 55,2 кДж/моль. Реакция идет до конца при 5—7-кратном избытке воды. Поэтому наиболее перспективно использование иадпе — рекисей там, где нет больших ограничений по тепловыделению и использованию воды, например в энергоустановках морского назначения.
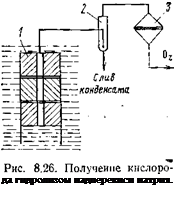
Генераторы кислорода работают по принципу аппарата Киппа — скорость подачи воды иа реакцию пропорциональна скорости потребления газа. Вся система работает следующим образом (рис. 8.26): вода поступает снизу в генератор кислорода /, вступает в реакцию с надперекисью, образовавшийся газ через центральное отверстие идет в отбойник 2, где происходит отделение капель влаги, а затем в фильтр 3, где газ отделяется от аэрозоля щелочи. Чистый кислород направляется через редуктор в ЭХГ. Образующийся раствор щелочи периодически сливается, а в конструкциях, работающих под водой, удаляется самотеком за счет разности удельных весов воды и раствора.