 Какой лёд лучше?
Какой лёд лучше?
Какой лёд лучше?
При замораживании воды в пластмассовых бутылках приметно, что поначалу возникает прозрачный лёд, как слеза, а в центре бутылки, в последнюю очередь замерзания, появляется мутный, непрозрачный лёд. Какие характеристики этих 2-ух видов льда и какой лучше употреблять после размораживания?
Ответ:
Замораживать воду идеальнее всего в посуде, сделанной из крепкого стекла. Для этого подойдёт неважно какая ёмкость – банка, кастрюля и т.д. и т.п. А ответ на ваш вопрос почему лёд кристаллизуется таким макаром состоит в том, что перевоплощение воды в кристалл происходит в первую очередь на центрах кристаллизации; примесях и неоднородностях — частицах пыли, пузырьках воздуха, мелких царапинах на стенках сосуда. Незапятнанная вода центров кристаллизации фактически лишена, потому она может переохлаждаться, и довольно очень, оставаясь водянистой, но мелкие пузырьки воздуха вода всегда содержит. Они то и являются предпосылкой наблюдаемого эффекта.
Есть даже такая догадка, что в структуре льда остаются бессчетные поры и промежутки, заполненные воздухом. Пузырьки воздуха вмерзают в лёд, и такая „губка“ становится существенно легче воды. Но даже лёд без микроскопичных пор и трещин имеет плотность 0,9168 г/см 3 при 0°С, а вода при той же температуре — 0,9984 г/см 3.
Лёд – это самая таинственная и необыкновенная после воды субстанция. На данный момент понятно 14 модификаций льда. Правда, все, не считая обычного нам льда, кристаллизующего в гексагональной сингонии и обозначающегося как лёд I , образуются в критериях экзотичных — при очень низких температурах (порядка -110150 0С) и больших давлениях, когда углы водородных связей в молекуле воды меняются и образуются системы, хорошие от гексагональной. Такие условия напоминают галлактические и не встречаются на Земле. К примеру, при температуре ниже –110 °С водяные пары выпадают на железной пластинке в виде октаэдров и кубиков размером в несколько нанометров — это так именуемый кубический лед. Если температура чуток выше –110 °С, а концентрация пара очень мала, на пластинке формируется слой только плотного бесформенного льда. Эта форма льда в свою очередь может самопроизвольно перебегать в гексагональный лёд, причём тем резвее, чем выше температура.
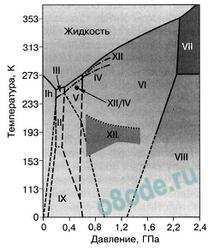 Рис. Диаграмма состояния кристаллических льдов
Рис. Диаграмма состояния кристаллических льдов
Две самых последние модификации льда — XIII и XIV — открыли ученые из Оксфорда совершенно не так давно, в 2006 году. Предположение о том, что должны существовать кристаллы льда с моноклинной и ромбической решетками, было тяжело подтвердить: вязкость воды при температуре –160°С очень высока, и собраться совместно молекулам незапятанной переохлажденной воды в таком количестве, чтоб образовался эмбрион кристалла, тяжело. Этого удалось достигнуть при помощи катализатора — соляной кислоты, которая повысила подвижность молекул воды при низких температурах. В земной природе подобные модификации льда создаваться не могут, но они могут встречаться на замерзших спутниках других планет. Более тщательно обо всём этом читайте на нашем веб-сайте.
Сами молекулы воды, состоящие из одного атома кислорода и двух атомов водорода, имеют вид шариков с выпуклостями. В кристалле льда они размещаются так, что неровности (надлежащие атомам водорода) ориентируются строго по направлению 2-ух примыкающих молекул. В результате появляется трёхмерная кристаллическая решётка, состоящая из почти безупречных тетраэдров. Любая молекула в его верхушках окружена 4-мя другими, т.е. имеет координационное число равное 4.
Рис. 1. Кристаллическая решётка льда. Молекулы воды H2O с атомом кислорода (красноватый шарик) и 2-мя атомами водорода (голубые шарики) в её узлах размещены так, что любая имеет четырёх „соседок“.
Похожие явления кристаллизации льда на примесях можно следить и в природе. Многие путники издавна отмечали, что глубочайшей осенью очень незапятнанные речки и ручьи начинают леденеть со дна. Через слой незапятанной воды отлично видно, что водные растения и коряги на дне зарастают рыхловатой ледяной шубой. В какой-то момент этот донный лёд всплывает, и поверхность воды одномоментно оказывается скованной ледяной коркой.
К подобным сообщениям всегда относились достаточно скептически. Температура верхних слоёв воды ниже, чем глубинных, и замерзание вроде бы должно начинаться с поверхности. Но незапятнанная вода леденеет без охоты, и лёд в первую очередь появляется там, где имеются центры кристаллизации — взвесь ила и твёрдая поверхность, — возле дна.
Кристалл льда стремится вырасти как можно более правильным — это „прибыльно“ с точки зрения его внутренней энергии. А любые примеси искажают форму решётки. Потому возрастающий кристалл теснит любые посторонние атомы и молекулы, стараясь строить безупречную решетку, пока это может быть. И только когда примесям деваться уже некуда, кристалл льда начинает встраивать их в свою структуру или оставляет в виде капсул концентрированной жидкостью. Потому морской лёд пресный, а даже самые грязные лужи покрываются прозрачным и чистым льдом.
Водопроводная вода содержит приблизительно 100 частей примесей на миллион частей воды (в главном это хлор, растворённый для дезинфекции, поваренная соль, которая есть всюду, и твёрдые наночастицы), также пузырьки расстворённого воздуха. Дистилляцией в обычных лабораторных критериях их количество несложно снизить раз в сто, получив воду с чистотой 99,9999%. Если же сосуд с этой водой медлительно охлаждать с одной стороны, получится лёд с чистотой уже до шести девяток после запятой. В нём отыщется только одна частичка примеси на сто миллионов частиц воды.
В минералогических коллекциях часто можно созидать, к примеру, прозрачные кристаллы корунда Al2O3, которые завершаются рубиновой „шапочкой“. Это возрастающий кристалл „собрал“ со всего объёма примесь — ионы хрома Cr 3+, которые превращают тусклый корунд в красный рубин.
Аналогичным образом, и лёд, выжимая примеси из своей кристаллической решётки, становится прозрачным. А снег же, который состоит из микроскопических кристалликов льда, непрозрачен. В чём же причина настолько различных оптических параметров 1-го и того же вещества?
Как это ни странно, причина тут одна. Лёд фактически не поглощает видимый свет. И если бы лёд не был прозрачным, снег не был бы белоснежным. Световые лучи проходят ледяную пластинку насквозь, а в слое снега испытывают неоднократное отражение и выходят назад, не потеряв ни одного из компонентов диапазона. Но если бы мы могли созидать инфракрасное излучение и ультрафиолет, снег казался бы нам полностью чёрным: коэффициент поглощения света в этих областях диапазона очень велик.
Не считая того, в воде содержатся мелкие пузырьки растворённого в ней воздуха. При замерзании воды они выделяются, вроде бы “прилипая” к граням кристаллов льда. Чем больше появляется кристалликов льда, тем больше пузырьков воздуха — вот вам и непрозрачный лед. В природе если вода подо льдом движется, воздушные пузырьки собираются совместно, и появляется прозрачный лед.
Прозрачный лёд можно сделать и в домашних критериях. Для этого необходимо использовать очень чистую, отлично прокипяченную (а еще лучше дистиллированную — она продается в аптеках) воду.
С почтением,
к.х.н. О.В. Мосин