 Способ меченых атомов
Способ меченых атомов
Способ меченых атомов
О.В. МОСИН
Техника меченых атомов заполучила широкую популярность в наше время. На теоретическом уровне эта методика очень ординарна. По существу, она сводится к введению особенного изотопа в на биологическом уровне принципиальный метаболит (либо продукт питания), после этого выслеживаются поочередные реакции этого метаболита в организме методом наблюдения за судьбой меченого изотопа в продуктах распада, крови, моче и т.д. На основании этих данных строится метаболизм. Внедрение меченых изотопов стало вероятным благодаря широкому развитию способов получения изотопов.
Большая часть хим частей в природных критериях существует в разных изотопных модификациях. Все изотопы данного хим элемента имеют однообразные хим характеристики, но различные атомные веса. Атомный вес изотопа равен сумме чисел нейтронов и протонов, находящихся в ядре. Хим характеристики элемента определяются только числом протонов, т. е. атомным номером. (благодаря различию в атомных весах два изотопа элемента могут характеризоваться несколько разными скоростями реакции.) К примеру, изотопы углерода, такие, как С11, С12 и С13, имеют 6 протонов и соответственно 5, 6 и 7 нейтронов в ядре.
Некие природные изотопы радиоактивны; они испускают или -частицы (ядра гелия Не4), или отрицательные -лучи (резвые электроны). Не считая того, многие радиоактивные изотопы испускают -излучение — фотоны высочайшей энергии.
 Большая часть искусственно приобретенных изотопов оказывается -активными (встречается как электрическая, так и позитронная -активность). В ряде всевозможных случаев бывает легче найти -излучение (фотоны), проваждающее распад, ежели -лучи (электроны). Искусственно приобретенные изотопы служат основой для био исследовательских работ с внедрением способа меченых атомов.
Большая часть искусственно приобретенных изотопов оказывается -активными (встречается как электрическая, так и позитронная -активность). В ряде всевозможных случаев бывает легче найти -излучение (фотоны), проваждающее распад, ежели -лучи (электроны). Искусственно приобретенные изотопы служат основой для био исследовательских работ с внедрением способа меченых атомов.
Таблица (справа). Некие изотопы, применяемые в биологии и химии.
Нерадиоактивные постоянные изотопы тоже могут быть применены в способе меченых атомов, позволяя поменять встречающиеся в природе изотопные соотношения. Содержание данного изотопа можно определять при помощи масс-спектрометрической техники. Используемые способы всераспространены на примере нерадиоактивного изотопа N15, который обычно встречается в концентрациях много наименьших, чем N14. Вводя соединения с высочайшим содержанием N15, можно приготовить эталоны метаболитов с излишком данного изотопа.
Обычно радиоактивный элемент употребляют в виде примеси в растворе — носителе, к примеру радиоактивный С14 употребляют растворенным в излишке нерадиоактивного С12. Такие соединения могут быть тогда использованы в системах, которые находятся в полном термодинамическом равновесии относительно атомов углерода, но дальних от равновесия относительно меченого изотопа. Способ меченых атомов позволяет учить сбалансированные био процессы без нарушения хим равновесия.
МЕЧЕНЫЕ АТОМЫ
В процессе опыта радиоактивные атомы распадаются. Распад данного атома представляет собой случайное событие; число распадов за секунду пропорционально числу радиоактивных атомов, имеющихся в реальный момент. В аналитической форме произнесенное записывается в виде
dN/dt = -N; (1)
где N — число радиоактивных атомов, имеющихся в данное время, t — время, N, — неизменная, соответствующая для избранного изотопа. Интегрируя уравнение (1), получаем
N = N0e-t (2)
где N0 — число .радиоактивных атомов в исходный момент. Из формулы (2) может быть определено время т, за которое число N миниатюризируется в два раза:
= ln2/ (3)
Время именуют периодом полураспада элемента. В течение каждого периода полураспада число атомов изотопа миниатюризируется вдвое.
Чтоб изотоп можно было использовать, применяя способ меченых атомов, должно быть в разумных границах. Если очень не достаточно (порядка секунд), то изотоп распадется до того, как можно будет поставить большая часть тестов. Но если очень велико, то число распадов за 1 сек получится неприемлимо низким для обнаружения обычно употребляемых концентраций меченых атомов. Изотоп С14 с периодом полураспада 5700 лет находится близко от этого нижнего предела.
Активность образцов радиоактивного материала выражают числом распадов за секунду. Число распадов, происходящих в 1 г радия за 1 сек, равное 3,7-1010, именуют кюри. Для био исследовательских работ при помощи меченых атомов более комфортно использовать одну тысячную этой единицы, т. е. милликюри. Число атомов на 1 мкюри связано с периодом полураспада. Если имеется 1 кюри данного радиоактивного изотопа, то
N = /ln2 x З,7-107 атомов.
Радиоактивные изотопы идентифицируют по их характеристическому излучению. В случае искусственных радиоактивных изотопов оно обычно складывается из -лучей и из -излучения. В случае орбитального электрического захвата (когда один из электронов поглощается ядром с уменьшением атомного номера на единицу) испускаются только фотоны. Чертой излучения данного изотопа является наибольшая энергия -лучей и энергия -излучения (фотонов). Комфортными единицами измерения при всем этом являются электрон-вольты (эв), килоэлектрон-вольты (кэв) либо мегаэлектрон-вольты (Мэв); 1 эв — это энергия, приобретаемая электроном в итоге прохождения ускоряющей разности потенциалов в 1 в2).
Частички, испускаемые в итоге радиоактивного распада, обнаруживаются с помощью специального сенсора излучения. Его показания могут быть потом подсчитаны при помощи хоть какой электрической схемы. В прошедшем более обширно всераспространенным типом сенсора была трубка Гейгера — Мюллера, именуемая счетчиком Гейгера. Он состоит из цилиндрической камеры, заполненной газом, с натянутой по ее оси проволокой (рис. 1). Проволока изолирована от наружного цилиндра и находится под высочайшим потенциалом. Ионизирующие частички, попадая в счетчик, вызывают лавинную ионизацию в газе; если к счетчику приложена довольно высочайшая разность потенциалов, возникающий импульс ионизационного тока будет зарегистрирован.
Рис. 1. Счётчик Гейгера.
В конструкции счётчиков Гейгера используются трубки различного поперечника – от нескольких мм до 25 см. Длина трубки колеблется от 1 до 50 см. Газ, наполняющий счетчик, геометрия устройств и чистота материала стен — все это оказывает влияние на работу счетчика. Импульсы счетчика Гейгера считают с помощью электрических схем. Обычно показания снимают с групп светодиодов, с электрического табло либо с картонной ленты. Другие электрические схемы позволяют производить конкретный счет импульсов.
Другим типом сенсора радиоактивного излучения является сцинтилляционный счетчик. Механизм работы этого счетчика основан на использовании мелких вспышек света, образующихся при попадании ионизирующего излучения во многие типы кристаллов и жидкостей. Спектральный состав излучения этих вспышек характерен для данного сцинтиллятора. Интенсивность сцинтилляционных вспышек пропорциональна энергии, израсходованной частичкой. Сцинтилляцию в свою очередь обнаруживают при помощи фотоумножителя, выходной сигнал которого поступает на амплитудный анализатор. Таким макаром, определенный изотоп может быть выделен из консистенции либо на фоне «шумов».
Сцинтилляционные счетчики могут быть сделаны разных размеров и формы. Пропорциональность выходного сигнала энергии частички в данном случае более строгая, чем для газового пропорционального счетчика. Применение жидкостных сцинтилляционных счетчиков позволяет растворять эталоны, имеющие низкую интенсивность либо же низкую энергию излучения, потому что в данном случае для регистрации употребляется излучение, испускаемое во всех направлениях. Для обнаружения -излучения сцинтилляционные счетчики более эффективны, чем счетчики Гейгера. Но в определенных случаях счетчики Гейгера имеют несколько наилучшее отношение сигнала к шуму, чем большая часть других сцинтилляционных счетчиков.
В неких случаях не так принципиально точно знать скорость распада, как узнать, в какой части клеточки локализован изотоп. Подобная задачка появляется в картонной хроматографии, когда разные соединения распределяются на поверхности кусочка фильтровальной бумаги. Дальше лучше отыскать на бумаге рассредотачивание радиоактивных участков. Чтоб их найти, можно поместить срез ткани (либо фильтровальную бумагу) на кусочке фотобумаги. Она будет засвечена излучением, а потом при проявлении позволит найти локализацию радиоактивных изотопов. Таковой снимок именуют радиоавтографом.
Хоть какой из этих способов регистрации может быть применен для хоть какого изотопа. Хотя понятно существование радиоактивных изотопов для всех частей, в био исследовательских работах употребляют только ограниченное их число. К более известным относятся С14, J131 и Р32.
ИЗОТОП УГЛЕРОДА С14
Встречающийся в природе углерод практически стопроцентно состоит из размеренного изотопа С12. Не считая того, всегда имеется малость (около 1%) размеренного изотопа С13 и ничтожное количество радиоактивного изотопа С14. Искусственным методом можно получить изотоп С14, также радиоактивные изотопы С10 и С11. Изотопы С10 и С11 имеют период полураспада соответственно 19 сек и 20,5 мин; при распаде оба изотопа испускают положительные -лучи и образуют изотопы бериллия (Be). Их периоды полураспада так коротки, что в био исследовательских работах с внедрением меченых атомов используют только радиоактивный изотоп углерода С14. Потому что углерод является значимой частью всех био соединений, то изотоп С14 употребляется очень обширно. Получить изотоп С14 можно при помощи ряда реакций. Если углерод, обогащенный изотопом С13, бомбить нейтронами, то некая его часть преобразуется в С14 за счёт реакции.
C13 + n 1 ——C14 +
Если углерод, обогащенный С13, бомбить дейтронами, то появляется С14:
C13 + D ——C14 + H1
Ни одну из этих реакций нельзя считать комфортной, потому что для концентрации С13, а потом и С14 должен быть применен масс-спектрометр.
Более действенная реакция получения изотопа С14 состоит в бомбардировке N14 нейтронами:
N14 + n1 ——C14 + H1
Соединения нитрат аммония (NH4NO3) и нитрит бериллия (BeNO2) нередко употребляют как источники азота. Потом изотоп С14 может быть выделен стандартными химическими способами. Некое количество его появляется таким методом в итоге деяния галлактических лучей на N14 в атмосфере, что дает около 10 отсчетов в 1 мин на 1 г углерода, находящийся в равновесии с атмосферным СО2.
Период полураспада С14 составляет около 5760 лет. Поэтоиу, для получения измеримого числа отсчетов нужна высочайшая концентрация этого изотопа. При распаде С14 испускает только электроны и преобразуется в N14; испускание -излучения отсутствует. Наибольшая энергия электронов составляет приблизительно 0, 154 Мэв. Данная величина сравнима с энергией фотонов, излучаемых мед рентгеновской трубкой, и меньше энергии частиц многих других радиоактивных изотопов. Используются разные методы регистрации этих электронов. Время от времени эталон, содержащий С14, заделывают в пилюлю карбоната бария (ВаСО3) и помещают снутри счетчика Гейгера. Разработаны особые счетчики Гейгера, созданные для заполнения их изотопом С14 в виде газа 14СО2. Употребляются также разные водянистые сцинтилляторы . Во всех случаях эталон не должен быть очень толстым, потому что все испускаемые им -лучи поглощаются при прохождении через несколько мм твердого либо водянистого вещества эталона.
Изотоп С14 имеет огромное значение при проведении исследовательских работ. Исследование синтеза протопорфирина и определение возраста органических веществ с помощью углерода — два соответствующих примера использования изотопа С14.
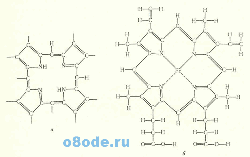 Протопорфирин является частью геминовой группы, которая представляет собой простетическую группу гемоглобина и неких ферментов (рис. 2).
Протопорфирин является частью геминовой группы, которая представляет собой простетическую группу гемоглобина и неких ферментов (рис. 2).
Рис. 2. Основная порфириновая структура (а) и железопротопорфирин IX (б).
Основная порфириновая структура представляет собой простетическую группу, общую для гемоглобина, миоглобина, каталазы, пероксидазы и цитохромов. Была также найдена в хлорофилле. К восьми «свободным» связям присоединяются разные группы. Железопорфирин IX (основная часть многих геминовых белков) содержится в составе гемоглобина, миоглобина и каталазы. Другие геминовые белки несут или эту порфириновую структуру, или ее производное, образованное ординарными подменами. Атом железа находится в закисной форме в восстановленном и оксигемоглобине, также в восстановленном и оксимиоглобине. В пероксидазе железо находится в окисном состоянии. У других геминовых белков атом железа в продолжение реакции может поочерёдно восстанавливаться и окисляться.
При помощи ряда тестов показано, что при образовании протопорфирина употребляется аминокислота глицин. Соответственно этому было приготовлено две формы глицина (звездочкой обозначен меченый атом, в этом случае С14).
При использовании первой модификации было найдено, что радиоактивность врубается в порфириновое кольцо, тогда как при использовании 2-ой формы этот эффект не обнаруживался. Эти опыты проявили, что глицин участвует в биосинтезе протопорфирина, но что углерод карбоксильной группы [СООН] с синтезом не связан. Хотя этот пример кажется очень обычным, было бы нереально узнать роль глицина любым другим способом, не считая использования меченых атомов. Опыты с изотопом N1B также указывают на то, что глицин является предшественником протопорфирина.
Броским примером использования меченых атомов может служить определение геологического возраста при помощи углерода. В данном случае измеряется радиоактивность древесной породы либо других органических материалов. Если эти материалы составляют часть системы не так давно бывшей живой, то ее атомы углерода будут находиться в динамическом равновесии с СО2 атмосферы; в итоге за счет изотопа С14 галлактического происхождения эталон будет давать около 10 отсчетов в 1 мин на 1 г углерода. В таком же веществе, но уже в течение долгого времени не живом и, как следует, не находящемся в равновесии с СО2 атмосферы, изотоп С14 равномерно распадается и не восстанавливается. Таким макаром, следует ждать, что кусочек кости мамонта, имеющей возраст около 5760 лет, содержит вдвое меньше С14 на 1 г углерода по сопоставлению с не так давно появившимся живым материалом. А кусочек древесной породы в возрасте 11 500 лет должен содержать вчетверо меньше этого же количества (т. е. давать 2,5 отсчета в 1 мин на 1 г углерода). Благодаря изотопу С14 появляется слабенькая радиоактивность с низкой интенсивностью. Все же можно с ювелирной точностью измерить содержание С14, подабающим образом отделив отсчеты, возникающие за счет галлактических лучей, распада другого рода, радиоактивного фона комнаты и электрических шумов. Когда удается сопоставить данные, приобретенные при помощи С14, сданными, приобретенными любым другим методом, то находится, что они согласуются вместе в границах экспериментальной ошибки. Для объектов, содержащих углерод и имеющих возраст от 2000 до 50 000 лет, данные, приобретенные при помощи изотопа С14, могут быть вычислены более точно, чем при помощи всех других способов. Возраст многих объектов, имеющих значение для археологии, антропологии и эволюции, можно найти только при помощи изотопа С14.
ИЗОТОП ЙОДА J131
Размеренный йод, встречающийся в природе, состоит приемущественно из изотопа J127. Известны многие радиоактивные изотопы йода: J128, J129, J130 и J131. Период полураспада изотопа J128 равен 25 мин, а изотопа J130—12 час. Оба нареченных изотопа употребляют в био исследовательских работах, но для большинства тестов они очень короткоживущие. Изотоп J129 имеет период полураспада около 107 лет, что очень много для удачного его внедрения в качестве радиоактивного индикатора. Очень комфортную длительность жизни (8 дней) имеет изотоп J131, владеющий много более высочайшей скоростью распада на грамм-атом, чем изотоп С14. В течение нескольких месяцев изотоп J131 практически стопроцентно распадается и уже не представляет вреда для здоровья. Вследствие его недлинного периода полураспада количество приобретенных отсчетов всегда нужно рассматривать как функцию той части начального количества, которая еще не распалась.
При распаде изотоп J131 испускает много частиц: электроны с наибольшей энергией 0,6 и 0,3 Мэв, также -кванты с энергией 0,08, 0,28, 0,37 и 0,64 Мэв. Два последних типа -излучения просто проходят через ткани и дюралевые фольги и могут быть свободно обнаружены. Окружив сенсор железным экраном, можно снизить естественный фон, не снижая чрезвычайно чувствительность к -излучению.
Изотоп J131 можно получить, бомбардируя J130 нейтронами. Более удачный способ заключается в бомбардировке нейтронами изотопа Те130. Этим методом получают J131, который может быть выделен с большой степенью чистоты посреди всех других частей. Основное количество изотопа J131 получают из товаров деления. Для использования в био исследовательских работах изотоп J131 обычно превращают в йодид какого-нибудь металла.
Для позвоночных йод является принципиальным метаболитом, потому что он составляет часть гормонов щитовидной железы. Его концентрация в щитовидной железе в 10 000 раз больше, чем в любом другом органе. Человеку раз в день нужно только очень маленькое количество йода (примерно 100 мкг). Если, но, он содержится в еде в наименьшем количестве, то у человека появляются разные заболевания щитовидной железы.
Радиоактивный Jl3l употребляют для того, чтоб проследить прохождение йода, начиная с момента его заглатывания, попадания в щитовидную железу, рассредотачивания в гормонах, по всему организму и до окончательного выделения. В особенности принципиальным примером является исследование поглощения щитовидной железой йода, введенного внутривенно. До использования изотопа было нереально показать протекание этого процесса у человека.
Проведены опыты, в каких разные количества изотопа J131 были введены морским свинкам, крысам, собакам и людям. В любом случае при маленьких инъекциях йодида большая его часть, а время от времени даже все введенное количество .в течение 24 час концентрировалось в щитовидной железе. При больших «фармакологических» дозах (около 5 ms. J131 на 1 кг живого веса) щитовидная железа концентрирует маленькую часть введенного йодида в течение первых 5 мин, после этого наступает насыщение. Содержание организма на сверхвысокой йодной диете также вызывает насыщение щитовидной железы. Опыты с применением ингибиторов демонстрируют, что железа концентрирует йодид как такой, даже если у нее подавлено образование ди-йодо-тирозина и тироксина. При помощи этих тестов показано, что щитовидная железа людей, питающихся обычной едой, не насыщена йодом, но в состоянии поглотить его в относительно большенных концентрациях (по последней мере 500 : 1 для йодидового коэффициента кровь/щитовидная железа),
ИЗОТОП ФОСФОРА Р32
Фосфор — это важная составная часть всякого живого организма. Он является значимым элементом нуклеиновых кислот, которые переносят генетическую информацию и определяют синтез белков. Живы клеточки употребляют фосфор в АТФ (аденозинтрифосфате) — соединении, которое является хранилищем энергии. Он играет важную роль в почти всех окислительных и восстановительных процессах. Фосфат кальция является основной составляющей частью костей. В природе фосфор существует исключительно в виде Р31. Он имеет на биологическом уровне принципиальный изотоп Р32. Его получают на ядерных реакторах из серы при помощи реакции
S32 + n1 ——H32 + H1
Изотоп Р32 имеет период полураспада 14,3 денька. Как и J131, он комфортен в применении, так как его период полураспада довольно велик, что позволяет проводить с этим изотопом опыты, но в то же время он довольно мал, что обеспечивает просто измеряемую интенсивность распада. Как изотоп С14, так и изотоп Р32 испускают электроны. Электроны, испускаемые изотопом С14, сравнимо тяжело найти, потому что их наибольшая энергия составляет только около 0,15 Мэв; наибольшая энергия электронов, испускаемых изотопом Р32, равна 1,7 Мэв, потому они обнаруживаются совсем не сложно.
Радиоактивные атомы изотопа Р32 использовались для исследования скорости синтеза дезоксирибонуклеиновой кислоты (ДНК) и рибонуклеиновой кислоты (РНК). В ткани мозга в течение 1-го денька поновой появляется наименее 1% ДНК, в ткани печени — примерно 1 %, а в мукозе тонких кишок — до 15%. Это свидетельствует о том, что в клеточках, которые не плодятся стремительно, происходит сравнимо малый обмен ДНК. В эмбриональной и раковой тканях скорость восстановления (либо синтезирования поновой) ДНК даже выше, чем в мукозе тонких кишок. Эти данные, меж иным, конкретно указывают на связь ДНК с генетической информацией.
РНК синтезируется существенно резвее ДНК во всех тканях, кроме стремительно возрастающих. Хотя скорость синтеза РНК несколько выше в мукозе тонких кишок, чем в печени, они различаются в данном случае только в 2—3 раза, тогда как разница меж скоростями синтезов ДНК добивается 15 раз. Эти данные находятся в Согласии с представлением о том, что РНК не несет прямой ответственности за передачу генетической инфы.
Постоянные ИЗОТОПЫ
В качестве меченых атомов, не считая радиоактивных, могут быть применены и редчайшие постоянные изотопы. Для измерения относительной распространенности размеренных изотопов употребляют масс-спектрометр (рис. 3).
Рис. 3. Схема масс-спектрометра.
1 – ионизационная камера; 2 – область ускорения; 3 – магнитный спектрометр скоростей; 4 – сенсор; А – анод; С – катод с отверстием; Е – электрод, находящийся под высочайшим отрицательным потенциалом; H – магнитное поле; T – мишень.
При масс-спектрометрическом анализе исследуемый материал поначалу должен быть преобразован в летучий газ, который потом подается при низком давлении в зону, где его бомбят электронами; это происходит в ионизационной камере (область 1 на рис. 3). Бомбардировка электронами приводит к выбиванию валентных электронов из атомов, которые, таким макаром, преобразуются в положительные ионы. Эти положительные ионы, если давление газа довольно низкое, ускоряются по направлению к катоду. Они проходят через отверстие в катоде и ускоряются высочайшим напряжением меж катодом и электродом А (рис. 3). Все однозарядные ионы получают схожую кинетическую энергию Е:
E = ? mv2
Скорость же ионов различна для каждого изотопа. Потом ионы делятся в согласовании с величиной скорости методом отличия в магнитном поле либо при помощи других средств и совсем масс-спектрометр может, быть применен для разделения изотопов либо для определения концентрации изотопов. Масс-спектрометр больше и труднее сцинтилляционного счетчика, но в принципе его внедрение не заносит дополнительных заморочек.
ИЗОТОП АЗОТА N15
Азот N15 содержится во всех живых организмах, он найден в почти всех строй блоках — био полимерах, таких, как аминокислоты, пурины, пиримидины, порфирины и флавины. Аминокислоты являются единицами, из которых полимеризуются белки; таким макаром, все белки содержат азот. Точно так же нуклеиновые кислоты, ДНК и РНК содержат пурины и пиримидины, а как следует, и азот.
Встречающийся в природе азот состоит из изотопов N14 (99,64%) и N16 (0,36%). Так как природная распространенность изотопа N15 так мала, он очень подходит для исследовательских работ с внедрением размеренных изотопов. Долгоживущий радиоактивный изотоп N13 имеет период полураспада только 10 мин, потому его можно использовать только в ограниченном числе тестов. Изотоп N16 является единственным, который применяется в большинстве био исследовательских работ, использующих азот для способа меченых атомов.
 Одним из примеров использования изотопа N14 было включение аминокислоты глицина в протопорфирин, в геминовую группу и в гемоглобин (рис. 4). Гемоглобин, меченный N16, потом был применен для определения среднего времени жизни эритроцитов.
Одним из примеров использования изотопа N14 было включение аминокислоты глицина в протопорфирин, в геминовую группу и в гемоглобин (рис. 4). Гемоглобин, меченный N16, потом был применен для определения среднего времени жизни эритроцитов.
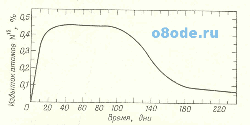
Рис. 4. Опыт с меченными атомами гемоглобина эритроцитов человека. Фиксируется избыток изотопа N15 в геминовой группе эритроцитов человека, получавшего в течение 3 дней меченый N15 глицин (рис. Из книжки Ю. Аккермана Биофизика, М., Мир, 1964).
При этих исследовательских работах подвергавшихся тесту людей кормили в течение 3 дней глицином, меченным N15 (рис. 4). При всем этом излишек N15 стремительно встраивался в геминовую группу эритроцитов. Эти данные использовались для определения скорости «рождения» новых клеток. Используя этот график, исследователи рассчитали среднее время жизни эритроцитов человека, которая равна примерно 127 денькам.
Таким макаром, в способе меченых атомов необыкновенные изотопы употребляются многими различными методами. Способности использования определённых меченых атомов зависят от их доступности, периода полураспада, энергии товаров распада, наличия подходящего для регистрации оборудования и концентрации элемента в живой системе.
ЛИТЕРАТУРА
Advances in Biological and Medical Physics, ed. by J. H. Lawrence and,?J. G. Hamilton, New York, Vol. 1, 1948; Vol. 2, 1951.
Advances in Biological and Medical Physics, ed. by J. H, Lawrence and?C. A. Tobias, New York, Vol. 3, 1953.
А г n о f f S., Techniques of Radmbiochemistry, Ames, Iowa, 1956.
Co mar C. L., Radioisotopes in Biology and Agriculture: Principles?and Practice, New York, 1955.
К a m e n M. D., Radioactive Tracers in Biology, 2nd ed., New York, 1951.
Strominger D., Hollander J. D., S e a b о г g G. Т., «Table?of Isotopes», Rev. Mod. Phys., 30, 42, Pt. II, 585 (1958).